Supstance prema intenzitetu boje rastvora (tačnije, prema apsorpciji svetlosti rastvorima).
Osnovne informacije
Jedan od prvih kolorimetara, koji je napravio francuski optičar Jules Dubosque, 1880.
Kolorimetrija je metoda za kvantitativno određivanje sadržaja supstanci u rastvorima, bilo vizuelno ili pomoću instrumenata kao što su kolorimetri.
Kolorimetrija se može koristiti za kvantificiranje svih onih supstanci koje daju obojene otopine, ili se može, pomoću kemijske reakcije, dati obojeno topljivo jedinjenje. Kolorimetrijske metode se zasnivaju na poređenju intenziteta boje ispitivanog rastvora, proučavanog u propuštenoj svetlosti, sa bojom referentnog rastvora koji sadrži strogo definisanu količinu iste obojene supstance, ili sa destilovanom vodom.
Zanimljiva je povijest nastanka kolorimetrije i fotometrije. Yu. A. Zolotov spominje da je Robert Boyle (baš kao i neki naučnici prije njega) koristio ekstrakt tanina da razlikuje željezo i bakar u otopini. Međutim, očito je Boyle prvi primijetio da što je više željeza sadržano u otopini, to je intenzivnija boja potonjeg. Ovo je bio prvi korak ka kolorimetriji. A prvi kolorimetrijski instrument bio je kolorimetar tipa Dubosque (1870), koji se koristio do nedavno.
Fotokolorimetri i spektrofotometri mjere količinu svjetlosti koja se prenosi na određenoj talasnoj dužini svjetlosti. Za kalibraciju uređaja koristi se kontrola (obično destilovana voda ili sirovi materijal bez dodanih reagensa).
Kolorimetrija se široko koristi u analitičkoj hemiji, uključujući hidrohemijsku analizu, posebno za kvantitativnu analizu sadržaja hranljivih materija u prirodnim vodama, za merenje, u medicini, a takođe i u industriji za kontrolu kvaliteta proizvoda.
Fotokolorimetrija
Fotokolorimetrija- kvantitativno određivanje koncentracije tvari apsorpcijom svjetlosti u vidljivom i bliskom ultraljubičastom području spektra. Apsorpcija svjetlosti se mjeri fotokolorimetrima ili spektrofotometrima.
Bilješke
Wikimedia fondacija. 2010 .
Pogledajte šta je "Kolorimetrija (hemijska metoda)" u drugim rječnicima:
Ne treba se brkati sa kalorimetrijom. Kolorimetrija (od latinskog boja boja i grčkog μετρεω mjerim): Kolorimetrija (nauka) je nauka o mjerenju boja. Kolorimetrija (hemijska metoda) metoda hemijske analize ... Wikipedia
Proučava odnos između sastava i makroskopskih svojstava. sistema sastavljenih od nekoliko izvor u in (komponente). Za F. x. a. karakterističan je prikaz ovih zavisnosti grafički, u obliku dijagrama, sastav svojstva; koriste se i stolovi ... ... Chemical Encyclopedia
Sadržaj ... Wikipedia
Ovaj izraz ima druga značenja, pogledajte Hemija (značenja). Hemija (od arapskog کيمياء, za koju se pretpostavlja da je nastala od egipatske riječi km.t (crno), odakle je ime Egipat, crna zemlja i olovo "crno ... ... Wikipedia
Wikirečnik ima članak o "organskoj hemiji"
Ovaj izraz ima druga značenja, pogledajte Biohemija (značenja). Biohemija (biološka ili fiziološka hemija) je nauka o hemijskom sastavu živih ćelija i organizama i o hemijskim procesima koji su u osnovi njihove životne aktivnosti. ... ... Wikipedia.
- (od drugog grčkog γῆ "Zemlja" i od λόγος "učenje") nauka o sastavu, strukturi i obrascima razvoja Zemlje, drugih planeta Sunčevog sistema i njihovih prirodnih satelita. Sadržaj 1 Istorija geologije ... Wikipedia
Socijalni rad je profesionalna djelatnost u organizaciji pomoći i uzajamne pomoći osobama i grupama u teškim životnim situacijama, njihovoj psihosocijalnoj rehabilitaciji i integraciji. U svom najopštijem obliku, socijalni rad predstavlja ... ... Wikipediju
Opšti uslovi- Uslovi rubrike: Opšti pojmovi Apsolutno crno tijelo Apsolutni minimum Apsolutni pokazatelj korištenja resursa i uštede resursa... Enciklopedija pojmova, definicija i objašnjenja građevinskih materijala
Ovaj članak ili odjeljak treba revidirati. Molimo da poboljšate članak u skladu sa pravilima za pisanje članaka. Kvantna hemija je pravac ... Wikipedia
Kolorimetrija je jedna od najjednostavnijih metoda analize apsorpcije. Zasnovan je na promjeni nijansi boje ispitne otopine ovisno o koncentraciji. Kolorimetrijske metode se mogu podijeliti na vizuelna kolorimetrija i fotokolorimetrija.
vizuelna kolorimetrija
Izvodi se na račun standardnih serija. Da biste to učinili, ispitna otopina se uspoređuje sa setom standardnih otopina, koji moraju biti svježe pripremljeni i međusobno se razlikovati za najmanje 10-15%.
Na primjer, kolorimetrijsko određivanje pH prema Aljamovskom zasniva se na svojstvu indikatora da mijenjaju svoju boju ovisno o koncentraciji vodikovih jona prisutnih u otopini.
Skala instrumenta Aljamovski je serija zatvorenih epruveta napunjenih obojenim rastvorom. Ova svjetlosno stabilna otopina oponaša boju univerzalnog indikatora pri određenom pH. Otopina za ispitivanje se upoređuje sa vagom i u njoj se nalazi epruveta koja joj najviše odgovara po boji. Ako se boja tečnosti ne poklapa sa bojom rastvora na skali, uzmite prosečnu vrednost između dve epruvete koje se po boji približavaju. Ponekad može postojati skup Aljamovskog, u kojem standardna skala boja nije predstavljena ampulama s otopinama, već staklenim pločama s obojenim filmovima.
Radi lakšeg poređenja, na uređaj je priključen komparator, ali je tehnika upoređivanja rješenja pomoću skale u ovom slučaju drugačija. Epruvetu sa obojenom otopinom za ispitivanje treba staviti u lijevu utičnicu komparatora. Sipajte 5 ml destilovane vode u epruvetu iz desnog priključka komparatora. U proreze komparatora ubacuje se standardna skala boja, pri čemu njen obojeni dio treba da bude uz epruvetu sa destilovanom vodom, a bezbojni dio uz ispitni rastvor. Komparator se uzima lijevom rukom i podiže u nivo očiju, držeći vagu dalje od sebe i okrećući je prema svjetlu. Pomerajući standardnu skalu gore-dole, pronađite njen deo koji odgovara boji test rastvora. Okrećući komparator sa skalom prema sebi, izbrojite pH vrijednost i zabilježite rezultat analize.
Fotokolorimetrija
Fotokolorimetrijske metode su jedna od široko korištenih varijanti apsorpcione optičke analize. Za preciznije određivanje analiziranog elementa koriste se posebni uređaji - fotoelektrokolorimetri (FEC).
Prilikom rada na FEC-u najčešće se koristi metoda kalibracione krive, zasnovana na konstrukciji kalibracionog grafika u osi "optička gustina - koncentracija" za standardne otopine poznate koncentracije. Mjerenjem optičke gustoće analizirane otopine iz grafikona se utvrđuje njena koncentracija. Za bolju asimilaciju fotokolorimetrijske metode studenti se pozivaju da na KFK-3-01 izvedu laboratorijsku analizu određivanja jona bakra i nikla u rastvoru ovom metodom.
Laboratorija 1
ODREĐIVANJE JONA TEŠKIH METALA U RASTOPU FOTOKOLORIMETRIJSKOM METODOM
Cilj: naučiće da radi na fotokolorimetru KFK-3-01. Odredite sadržaj jona teških metala na KFK-3-01.
Redoslijed rada na fotometru KFK-3-01.
Zatvorite poklopac odjeljka za kivetu. Uključite prekidač "Mreža". Nakon 30 minuta počnite sa radom. Postavite željenu talasnu dužinu.
- 1. Podešavanje talasnih dužina mora se izvršiti povezivanjem sa strane kratkih talasnih dužina na duže. Ukoliko je tokom ugradnje vrednost talasne dužine premašila potrebnu, potrebno je ponovo vratiti za 20-30 Nm na kraće talase i ponovo podesiti potrebnu vrednost.
- 2. Uzmite dvije kivete. U jednu sipajte destilovanu vodu, a u drugu test rastvor. Kivete su napunjene do oznake sa strane. Na vanjskoj površini kivete ne smije biti kapljica.
- 3. Postavite kivete u odjeljak za ćelije. Postavite kivetu sa “praznim uzorkom” u udaljenu utičnicu držača kivete. Postavite ručicu za kretanje kivete u krajnji lijevi položaj. Zatvorite poklopac odjeljka za kivetu.
- 4. Koristite tipku "D" ili "C" za odabir načina mjerenja. Pritisnite tipku "#". Na donjem indikatoru, na gornjoj liniji, nakon 3-5 s bit će upisano "Matura". Natpis će nestati i pojavit će se "Promjena", a rezultat mjerenja će se pojaviti u donjem redu. Postavite dugme za kretanje kivete udesno. Rezultat mjerenja (optička gustina testnog rastvora) će se pojaviti u donjem redu.
Zadatak 1. Određivanje sadržaja C++ u rastvoru fotokolorimetrijskom metodom.
Oprema i reagensi: fotometar KFK-3-01, kiveta 3 cm, volumetrijske tikvice 50 ml, pipete 5,10 ml, standardni rastvor Cu ++ - 0,5 mg/ml, rastvor amonijaka 1:1.
Eksperimentalna tehnika
1. Izbor talasne dužine.
U odmjernu tikvicu od 50 ml dodati 14 ml standardnog rastvora Cu +2, dodati 15 ml amonijaka i razblažiti vodom do oznake. Pomiješajte i izmjerite optičku gustinu rastvora /) iz talasne dužine x. Popunite tabelu. 1. Ta talasna dužina se uzima kao optimalna X 0, pri kojoj je vrijednost optičke gustoće maksimalna za dato rješenje (slika 1).
Rice. 1. Ovisnost optičke gustoće E na talasnoj dužini X
2.
U volumetrijskim tikvicama kapaciteta 50 ml pripremite 5-6 rastvora Cu - ^ sa različitim sadržajem od 1 do 7 mg / ml. Zapremina svakog rastvora je 15 ml. U svaku tikvicu dodati 15 ml amonijaka i razblažiti vodom do oznake. Pomiješajte i izmjerite optičku gustinu I na odabranoj talasnoj dužini X 0 . Popunite tabelu. 2 i nacrtajte zavisnost optičke gustine?) od koncentracije rastvora C (slika 2).

3. Određivanje sadržaja Cu +2 u kontrolnom rastvoru.
U tikvicu sa kontrolnim rastvorom dodati 10 ml vode, 15 ml amonijaka. Dovedite do oznake vodom i promiješajte. Izmjerite optičku gustinu otopine. Prema kalibracionom grafikonu (slika 2), odrediti C 0 - sadržaj Cu +2 u rastvoru.
4. Izvucite zaključke iz rada.
Zadatak 2. Određivanje sadržaja Na+2 u rastvoru fotokolorimetrijskom metodom.
Oprema i reagensi: fotometar KFK-3-01, kiveta 3 cm, volumetrijska tikvica 50 ml, pipete 5,10 ml, standardni rastvor 1Ch1++ - 0,01 mg/ml, 1% alkoholni rastvor dimetilglioksima, voda joda, rastvor amonijaka 1:1.
Eksperimentalna tehnika
1. Izbor talasne dužine.
U odmjernu tikvicu od 50 ml dodati 10 ml standardnog rastvora br., dodati 5 ml jodne vode, 6 ml amonijaka i 2 ml dimetilglioksima. Razrijediti vodom do oznake, promiješati. Nakon 5-7 minuta izmjerite optičku gustoću otopine na različitim talasnim dužinama. Popunite tabelu. 1. Nacrtajte zavisnost optičke gustine rastvora?> od talasne dužine x. Talasna dužina 7,0 na kojoj je vrijednost optičke gustoće maksimalna za dato rješenje uzima se kao optimalna (vidi sliku 1).
2. Konstrukcija kalibracionog grafikona.
U volumetrijskim tikvicama kapaciteta 50 ml pripremiti 5-6 rastvora br. +2 različitog sadržaja od 0,01 do 0,1 mg/ml. Zapremina svakog rastvora je 10 ml. Zatim dodajte reagense u svaku tikvicu, kao što je navedeno u paragrafu 1. Dovedite do oznake vodom, promiješajte. Nakon 5-7 minuta izmjerite optičku gustinu otopine na odabranoj talasnoj dužini. Popunite tabelu. 2 i nacrtajte zavisnost optičke gustoće O na koncentraciju otopine C (vidi sliku 2).
3. Definicija sadržaja № +2 u kontrolnom rastvoru.
Dodati 10 ml vode u tikvicu sa kontrolnim rastvorom, a zatim dodati reagense kao što je navedeno u paragrafu 1. Izmeriti /) 0 - optičku gustinu rastvora. Prema kalibracionom grafikonu (slika 3) C (), odrediti C 0 - sadržaj br. +2 u rastvoru.
4. Izvucite zaključke o radu.
Tabela 1
(Filin V.A. Videoecology. Šta je dobro za oko, a šta loše. M.: Videoekologiya, 1997).
Metode analize zasnovane na upoređivanju intenziteta boje ispitnog rastvora i rastvora određene koncentracije - standardne, nazivaju se kolorimetrijski (kolorimetrija). Razlikuju se vizualna kolorimetrija, koja se provodi uz pomoć oka promatrača, i fotoelektrična kolorimetrija koja se izvodi uz pomoć fotoćelije.
Ako se kroz sloj otopine prođe snop svjetlosti intenziteta I0, tada će se nakon prolaska kroz ovaj sloj intenzitet svjetlosti smanjiti na It. Jednačina osnovnog zakona kolorimetrije - Bouguer-Lambert-Beerov zakon - ima sljedeći oblik:
![]()
gdje je to intenzitet svjetlosnog toka nakon prolaska kroz otopinu koncentracije C i debljine sloja l; I0 - intenzitet padajućeg svetlosnog toka; g je koeficijent koji zavisi od talasne dužine upadne svetlosti, prirode otopljene supstance i temperature rastvora; koeficijent g se naziva molarni koeficijent ekstinkcije. Odnos intenziteta svetlosnog toka koji prolazi kroz rastvor It i intenziteta upadnog svetlosnog toka I0 naziva se transmisija ili prozirnost i označava se slovom T:

Vrijednost T, koja se odnosi na debljinu sloja od 1 cm, naziva se propusnost. Logaritam recipročne transmisije naziva se ekstinkcija (ektinkcija) E, ili optička gustina D:

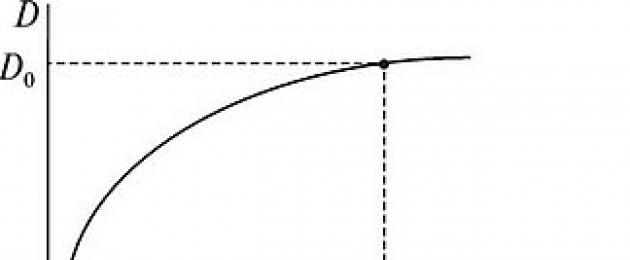
Stoga je otplata E direktno proporcionalna koncentraciji supstance u rastvoru. Ako grafički prikažemo zavisnost otplate od koncentracije, crtajući koncentraciju duž apscise, a otplatu duž ordinate, dobićemo pravu liniju koja se proteže od početka (Sl. 52).

Takav graf omogućava da se izvede zaključak o primjenjivosti osnovnog zakona kolorimetrije na proučavana rješenja. Ako se rješenje pridržava ovog zakona, onda graf koji izražava ovisnost otplate; iz koncentracije, biće predstavljen pravom linijom. Ako rješenje nije u skladu s ovim zakonom, tada se narušava ravnost u nekom dijelu krivine ili duž cijele njene dužine.
Metode vizuelne kolorimetrije
Vizuelna kolorimetrija se izvodi prema jednoj od sledećih metoda: 1) metodi standardnih serija; 2) kolorimetrijska titracija ili metoda dupliranja; 3) metoda izjednačavanja boja. Prva dva od njih ne zahtijevaju poštivanje osnovnog zakona kolorimetrije; metoda izjednačavanja boja zahtijeva podređivanje rješenja osnovnom zakonu kolorimetrije.

Metoda standardne serije
Suština metode. Kod kolorimetrije metodom standardnih serija, ispitna otopina u sloju određene debljine uspoređuje se sa skupom standardnih otopina iste debljine sloja, koji se međusobno razlikuju po intenzitetu boje za oko 10-15%. Nepoznata koncentracija jednaka je koncentraciji standardne otopine čija boja odgovara boji ispitne otopine ili je između dvije najbliže slabije ili jače obojene. Metoda standardne serije može se koristiti za određivanje sadržaja aldehida, fuzelnog ulja i metil alkohola u rektificiranom alkoholu. Boja se poredi u epruvetama sa brušenim čepovima istog prečnika od bezbojnog stakla iste debljine. Kolorimetrijske epruvete se postavljaju u poseban stalak (Sl. 53) i na pozadini matiranog stakla ili lista belog papira upoređuje se boja rastvora za ispitivanje sa bojom standardnih rastvora. Kada koristite cijevi s ravnim dnom, boje se mogu uporediti gledajući rješenja odozgo. Ovo je posebno korisno kada radite sa slabo obojenim brijačima.
1) standardni rastvori izoamil alkohola sa sadržajem 0,0005; 0,001; 0,002 i 0,003% vol. u 96% etanolu bez fuzelnog ulja i aldehida;
2) 0,05% rastvor paradimetilaminobenzaldehida u koncentrovanom x. uključujući sumpornu kiselinu sa relativnom gustinom od 1,835.
Napredak analize. Odmjeri se 0,5 ml ispitnog alkohola gradiranom pipetom na 1 ml i stavi u čistu, suhu tikvicu ravnog dna sa dugim grlom, u koju se iz mjernog cilindra doda 10 ml otopine paradimetilaminobenzaldehida. Sadržaj se pomeša, tikvica se uroni u ključalu vodenu kupelj i drži u ključaloj vodi tačno 20 minuta. Staklena čaša od 300 ml koristi se kao vodeno kupatilo. Grlo tikvice treba da bude u nagnutom položaju prilikom ključanja. Nakon 20 minuta, tikvica se brzo ohladi u tekućoj vodi. Istovremeno, sadržaj tikvice dobiva svijetlo žućkasto-ružičastu boju, koja prelazi u ružičastu različitog intenziteta, ovisno o sadržaju fuzelnog ulja.
Sadržaj tikvice se sipa u epruvetu sa brušenim čepom. Boja test alkohola se poredi sa bojom standardnih rastvora koji su podvrgnuti istom tretmanu kao i test alkohol. Podudaranjem boja određuje se sadržaj fuzelnog ulja u ispitnom alkoholu.
Metoda kolorimetrijske titracije
U kolorimetrijskoj metodi titracije određena zapremina obojenog rastvora nepoznate koncentracije koja se ispituje upoređuje se sa istom zapreminom vode kojoj se dodaje obojeni standardni rastvor određene koncentracije. Dodati rastvor iz birete (titrirati) dok boja ne bude jednaka ispitivanoj otopini. U tehnohemijskoj kontroli fermentacionih postrojenja ova metoda se koristi za određivanje boje piva koja se izražava u mililitrima 0,1 N. rastvor joda se dodaje u 100 ml destilovane vode da se boja izjednači sa 100 ml piva. Napredak. Ova definicija se provodi na sljedeći način. Dvije identične kemijske čaše kapaciteta 150-200 ml stavljaju se na list bijelog papira ili na bijeli porculanski tanjir. U jednu se sipa 100 ml piva, u drugu 100 ml destilovane vode. U čašu vode sipane iz birete uz miješanje 0,1 N. rastvor joda sve dok boja tečnosti ne postane ista kada se gleda odozgo i sa strane (kroz tečnost).
Metoda izjednačavanja boja
Zamislite da postoje dvije obojene otopine koje sadrže istu obojenu supstancu, ali u različitim koncentracijama. Iskupljenje svakog od rješenja bit će respektivno jednako
Promjenom debljine sloja ovih otopina (l) moguće je postići stanje u kojem će, uprkos različitim koncentracijama, intenzitet svjetlosnog toka koji prolazi kroz oba rješenja biti isti - doći će do optičke ravnoteže. To će se dogoditi kada oba rješenja apsorbuju isti dio svjetlosti, tj. kada će otplate rješenja biti jednake; u ovom slučaju, E1 = E2 i eC1l1 = eC2l2. Koeficijent ekstinkcije e oba rješenja je isti (rastvor sadrži istu supstancu). shodno tome,
![]()

one. debljine slojeva rastvora iste uočene boje obrnuto su proporcionalne koncentracijama rastvora. Ovaj odnos između debljine sloja i koncentracije je osnova metode izjednačavanja boja.

Izjednačavanje boja vrši se u posebnim uređajima - kolorimetrima. Vrlo uobičajen kolorimetar za uranjanje je Dubosque sistem. Optička šema ovog kolorimetra je sljedeća (Sl. 54). Svjetlosni tok iz ogledala 1 prolazi kroz sloj ispitne otopine u ćeliji 2, klip 4, prizmu 6, sočiva 8 i 9 i ulazi u okular, osvjetljavajući desnu polovinu optičkog polja. Drugi svjetlosni tok prolazi kroz sloj standardnog rastvora u ćeliji 3, klipu 5, prizmu 7, sočivima 8 i 9 i ulazi u okular, osvjetljavajući lijevu polovinu optičkog polja. Promjenom visine stupaca rješenja uz pomoć regala postiže se optička ravnoteža – nestanak međusklopa. Opšti izgled kolorimetra je prikazan na sl. 55.

Boju alkoholnih pića određuje kolometar, a to je imerzioni kolorimetar tipa Dubosque u kojem je jedna od kiveta zamijenjena okvirom na koji je postavljen odgovarajući standard suve boje. Standardi čvrste boje su acetatni film obojen trajnim hemijskim bojama.
Da bi se izmerila boja ispitivanog proizvoda, nakon filtracije, on se sipa u kivetu 1 kolomera (Sl. 56), a odgovarajući standard 2 se stavlja na poseban stalak. rastvora i standarda boje, ulazi kroz prizme 3 i 4 u komoru 5 sa dve prizme koje usmeravaju zrake svetlosti u teleskop 6. U teleskopu se posmatra polje čija je polovina osvetljena snopom koji prolazi kroz proizvod koji se proučava. Ujednačeno obojenje oba segmenta polja postiže se podizanjem ili spuštanjem kivete 1 uz pomoć nosača.
Nakon izjednačavanja boje u oba segmenta vidnog polja, visina stupca tečnosti u milimetrima se računa na skali uređaja i upoređuje sa visinom kolone odobrene za dati proizvod. Dakle, za liker od narandže koristi se standard br. 7, visina stupca na skali mjerača boja treba biti 33 mm, za čokoladni liker - standard br. 14, visina stupca je 26 mm. Navedeni podaci za sva alkoholna pića dati su u uputstvu za tehničku i hemijsku kontrolu proizvodnje alkoholnih pića. Ako su dobijene brojke jednake ili se međusobno razlikuju za ±5, tada se smatra da boja ispitivanog proizvoda odgovara odobrenom uzorku. Ako je rezultirajuća visina veća od odobrene, proizvod se premazuje, ako je manja, onda se ponovo farba.
Skup standarda uključuje bezbojne kompenzacijske filtere, koji se koriste za izjednačavanje prirodne svjetline boja nekih proizvoda sa svjetlinom boje filtera boje. Kompenzator se postavlja na svetlosnu rupu kolomera ispod kivete sa proizvodom.
Fotokolorimetrijska metoda
Ova metoda je opisana u poglavlju knjige "Tehnohemijska kontrola sušenja povrća i proizvodnje koncentrata hrane".
Kolorimetrijsko određivanje sadržaja ugljikohidrata u poluproizvodima proizvodnje alkohola (VNIISL metoda)
Reagens za određivanje sadržaja ugljenih hidrata kolorimetrijskom metodom u poluproizvodima proizvodnje alkohola je rastvor antrona u hemikaliji. uključujući sumpornu kiselinu sa relativnom gustinom od 1,830 (koncentracija od 0,2% tež.). U jako kiseloj sredini, glukoza se razgrađuje i formira derivate furfurala, koji reagiraju s antronom i formiraju zeleno kompleksno jedinjenje. Ovom metodom se utvrđuje ukupna količina ugljikohidrata, a podaci se dobijaju u jedinicama glukoze. Preliminarna hidroliza polisaharida u glukozu nije potrebna, jer se reakcija s antronom odvija u jako kiseloj sredini; u ovom slučaju, polisaharidi se hidroliziraju u monosaharide, koji reagiraju s antronom.

Za određivanje sadržaja ugljikohidrata potrebno je izgraditi kalibracijsku krivulju na x otopinama. uključujući glukozu u koncentraciji od 5-10 mg / 100 ml (slika 59). Kalibraciona kriva se gradi na sljedeći način. Pripremiti rješenja x. uključujući glukozu u koncentraciji od 5 do 10 mg u 100 ml otopine svaki miligram. Zatim se 5 ml reagensa sipa u vatrostalnu staklenu epruvetu od 20 ml i tu se pažljivo doda 2,5 ml pripremljenog rastvora glukoze tako da se formiraju dva sloja. Epruveta se zatvori brušenim čepom, njen sadržaj se brzo pomeša i epruveta se stavi u kipuću vodenu kupelj na 6 minuta. Nakon tog vremena, epruveta se izvadi iz kupke, reakciona smeša se ohladi na 20°C i obojeni rastvor se kolorimetrije u fotokolorimetru pomoću svetlosnog filtera sa svetlosnom talasnom dužinom od 610 nm i kivete sa dužinom lica od 5 mm. Mjerenja počinju s najkoncentriranijom otopinom (u ovom primjeru 10 mg glukoze u 100 ml otopine). Optička gustina se mjeri pomoću lijevog bubnja. Nakon mjerenja optičke gustoće svih rastvora, gradi se kalibraciona kriva, na kojoj su poznate koncentracije duž ose apscise, a odgovarajuće optičke gustoće duž ordinatne ose. Kao što se može vidjeti iz gornje krive (vidi sliku 59), optička gustina raste proporcionalno koncentraciji glukoze u otopini. Ova zavisnost se izražava ravnom linijom.
Za određivanje ugljikohidrata ispitni rastvor se razblaži do sadržaja od 5-10 mg u 100 ml rastvora i određivanje se vrši na ovaj način: 5 ml reakcione smeše se sipa u epruvetu, zatim 2,5 ml rastvora. test rastvor se pažljivo dodaje tako da se formiraju dva sloja. Ubuduće postupite kao kod konstrukcije kalibracione krive. Određivanjem optičke gustoće D duž kalibracijske linije, nalazi se sadržaj glukoze u otopini. Sadržaj glukoze u otopini također se može izračunati pomoću jednačine
![]()
koja je jednačina kalibracione linije i zasnovana je na koordinatama ove linije.
Tipično, optička gustoća se određuje u kiveti sa dužinom lica od 5 mm. Ako je otopina glukoze jako koncentrirana, tada će se nakon reakcije s antronom dobiti otopina preintenzivne boje, čija će optička gustoća biti veća od granične optičke gustoće bubnja fotokolorimetra i neće biti moguće odrediti njenu vrijednost; sa visoko razblaženim rastvorom glukoze, vrednost optičke gustine će biti mala, a greška u određivanju značajna. U oba slučaja, analizu treba ponoviti, shodno tome mijenjajući razrjeđenje otopine. Također je moguće, bez ponavljanja analize, odrediti optičku gustoću korištenjem druge kivete tokom kolorimetrije: za jako obojene otopine sa dužinom lica od 3 ili 1 mm, za slabo obojene otopine - 10 ili 20 mm. Nakon dobivanja optičke gustoće u drugim kivetama, nemoguće je odrediti sadržaj glukoze korištenjem kalibracijske linije povučene u odnosu na kivetu dužine lica od 5 mm. Potrebno je prethodno izračunati vrijednost optičke gustine otopine koja se dobije za ovu dužinu ruba kivete prema jednačini

gdje je D5 optička gustina otopine dobivene korištenjem kivete s dužinom lica od 5 mm; Dx je optička gustina rastvora dobijenog u kiveti sa dužinom lica od mm.
Ova metoda je primjenjiva na otopine koje sadrže ostatke glukoze u kojima nema pentoza i pentozana.
Određivanje sadržaja rastvorljivih nefermentisanih ugljikohidrata u zreloj kaši od zrna krompira (VNIISL metoda)
Zrela kaša od zrna krompira, uz ugljene hidrate koji se mogu pretvoriti u alkohol (skrob, dekstrini, maltoza, glukoza), sadrži i pentoze i pentozane, koji se ne pretvaraju u alkohol. Kada se odredi hemijskom metodom, utvrđuje se ukupna količina ugljikohidrata. U međuvremenu, vrlo je važno znati sadržaj fermentabilnih ugljikohidrata u kaši, koji su mogli fermentirati, a nisu fermentirali zbog nepotpune saharifikacije i fermentacije – tzv. nefermentiranih ugljikohidrata. Donedavno su se određivali razlikom između ukupne količine ugljikohidrata i pentoza; određivanje pentoza (vidi str. 82) je relativno teško i dugotrajno. Kolorimetrijska analiza omogućava direktno određivanje nefermentisanih ugljikohidrata u kaši.
Poznato je da antron mrlja svim ugljikohidratima, uključujući pentoze. Međutim, antronska reakcija je oko 12 puta manje osjetljiva u određivanju pentoza nego u analizi heksoza. VNIISL je razvio novu modifikaciju antronske metode, u kojoj je eliminisan uticaj pentoza i pentozana na rezultate analize. Ova modifikacija se zasniva na sljedećem zakonu kolorimetrije: optička gustoća mješavine komponenti jednaka je zbroju proizvoda koeficijenata ekstinkcije pojedinačnih komponenti i njihove koncentracije
gdje je D optička gustina smjese, jednaka lg0/l. Ovdje je l0 intenzitet početne svjetlosti; l je intenzitet svetlosti koja prolazi kroz rastvor; e1, e2, ..., en - omjeri otkupa;
Ovdje je D optička gustoća komponente, C je koncentracija komponente u otopini, l je dužina lica kivete.
Optička gustina rastvora zavisi od talasne dužine. Prilikom razvoja metode odabrana su dva talasa. Kod jednog od njih, prva komponenta (glukoza) ima intenzivnu traku, a druga (arabinoza) apsorbira vrlo slabo. Na drugoj talasnoj dužini, slika bi trebala biti obrnuta. Na osnovu sprovedenih studija, za kolorimetriju su izabrani svetlosni filteri talasne dužine svetlosti od 610 i 413 nm.
Određivanje sadržaja nefermentisanih ugljikohidrata u kaši provodi se na sljedeći način. Odvažite porciju od 25 g filtrata kaše u čaši, prebacite u odmjernu tikvicu od 200 ml. Čaša se ispere vodom i ispiranje se sipa u istu tikvicu. Zatim se u tikvicu doda 2 ml 30% rastvora cink sulfata radi bistrenja, meša, drži 2-3 minuta i doda se 2 ml 15% rastvora žute krvne soli i ponovo promeša. Zapremina rastvora je dovedena do oznake destilovanom vodom.
Rastvor se filtrira u suhu tikvicu. Prvih 20-30 ml filtrata se odbacuje, a naredni dijelovi se koriste za analizu. Filtrat se razrijedi drugi put tako da 100 ml otopine sadrži ugljikohidrate od 5 do 12 mg. Za određivanje, 10 ml antron reagensa se sipa u epruvetu od 20 ml sa brušenim čepom i pažljivo se doda 5 ml rastvora za ispitivanje da se tečnosti ne mešaju, već se dobijaju dva sloja; epruveta je zatvorena čepom. Paralelno, pripremite slijepu otopinu dodavanjem 5 ml destilovane vode u 10 ml reagensa. Sadržaj epruveta se snažno meša 10 sekundi i uroni u vodeno kupatilo koje je snažno ključalo. Vrenje bi trebalo da se nastavi u roku od 0,5 min od trenutka kada se epruvete urone u kadu. Primećuje se početak ključanja vode u kadi i ostavlja se da odstoji 5,5 minuta da se reakcija izvede. Nakon starenja, epruvete se hlade u kupelji s tekućom vodom do 20°C. Optička gustina dobijenog rastvora se određuje na levom bubnju fotoelektričnog kolorimetra pomoću dva svetlosna filtera: narandžastog sa talasnom dužinom L = 610 nm i plavo-ljubičasta sa talasnom dužinom L = 413 nm u kiveti sa dužinom lica od 5 mm. Kiveta se 2-3 puta ispere ispitnim rastvorom, a zatim se napuni tako da tečnost ne dođe do ivica za 5 mm. Vanjske stijenke kivete se peru mlazom vode i brišu suhim filter papirom. Na isti način, slijepa otopina se sipa u dvije druge kivete iste veličine i određuje se optička gustoća.
Prema vrijednostima optičke gustoće, sadržaj topivih nefermentiranih ugljikohidrata nalazi se prema jednadžbama:

gdje je D1 optička gustina sa svjetlosnim filterom s talasnom dužinom L = 610 nm; D2 - optička gustina sa svetlosnim filterom talasne dužine L = 413 nm; n je faktor razblaženja.
Kratke teorijske informacije Kolorimetrijske metode se zasnivaju na vizuelnoj proceni apsorpcije svetlosti rastvorima. Kolorimetrijska analiza je mali dio spektrofotometrijske analize. Najjednostavnije kolorimetrijske metode pojavile su se u 19. stoljeću (npr. metode za analizu mineralnih voda), ali se i danas u agrohemijskoj, hidrohemijskoj i kliničkoj analizi koriste ekspresne metode koje ne zahtijevaju instrumente i laboratorijsku opremu. Kolorimetrijske metode se koriste tamo gdje su brzina i niska cijena analize važniji od njene tačnosti. Imajte na umu da se u modernim kolorimetrijskim tehnikama koriste iste fotometrijske reakcije kao u instrumentalnim metodama za mjerenje apsorpcije svjetlosti.
Za procjenu koncentracije analita mogu se koristiti različite varijante kolorimetrijske analize.
1. Metoda standardne skale. Ovo je najčešća i najbrža od svih kolorimetrijskih metoda. U njemu se upoređuje vidljiva boja ispitnog rastvora u identičnim cilindrima ili epruvetama sa nizom obojenih rastvora istog sastava, ali sa poznatim sadržajem analita X. koncentracija X u ispitnom rastvoru, priprema se nova, detaljniju skalu za ovaj konkretan raspon koncentracije, a zatim precizirati rezultat analize koristeći je. Metoda standardne skale ne zahtijeva ispunjenje Beerovog zakona (za razliku od metode podešavanja) i daje grešku reda veličine 30% rel.
Budući da ljudsko oko mnogo bolje razlikuje nijanse boja od promjene intenziteta iste boje, metoda standardne skale daje bolje rezultate kada se rješenja koja formiraju standardnu skalu razlikuju u boji. Na primjer, organski reagens ditizon u odsustvu prijelaznih metala ima čistu zelenu boju, kompleks ditizona sa cinkom je crven, a otopine standardne skale koje sadrže različite količine cinka i istu količinu ditizona uzete u višku daju sve moguće međuboje između zelene i crvene. U takvim slučajevima, određivanje koncentracije metala na standardnoj skali nije inferiorno u točnosti mnogim instrumentalnim metodama (greška reda veličine 10%).
2. Kolorimetrijska titracija. Kod takve "titracije" ne dolazi do hemijskih reakcija, naziv je uslovno. Metoda se sastoji u tome da se iz ispitnog uzorka pripremi obojena otopina i ulije u određenu posudu, a standardna obojena otopina X poznate koncentracije (veća nego u uzorku) se postepeno dodaje u drugu sličnu posudu čistog rastvarača sve dok rastvori u boji ne budu jednaki oku. Budući da je debljina apsorbirajućeg sloja ista, vjeruje se da je nakon izjednačavanja boja koncentracija X u oba rješenja također ista. Prema zapremini upotrijebljene standardne otopine izračunava se koliko je tvari koja se treba odrediti bilo sadržano u uzorku.
3. metoda razblaživanja. Kod ove metode pripremaju se i testni i standardno obojeni rastvori, a zatim se onaj koji je intenzivnije obojen razblaži čistim rastvaračem dok (sa istom debljinom sloja rastvora!) njihove vidljive boje ne budu jednake. Znajući stepen razblaženja, izračunajte koncentraciju ispitne otopine.
4. Metoda izjednačavanja. Isti intenzitet apsorpcije svjetlosti kod proučavanih i standardnih rješenja ovdje se postiže promjenom debljine apsorbirajućeg sloja. To se može učiniti u posebnom uređaju - imerzionom kolorimetru ili jednostavno u paru cilindara, kada se gleda odozgo. Ako je hemijski sastav oba rastvora isti, Beerov zakon je zadovoljen, a vidljive boje (a samim tim i optičke gustine rastvora) su iste, možemo napisati:
D st \u003d e l st C st D x \u003d e l x C x C x \u003d C st l st / l x
Metoda izjednačavanja je preciznija od ostalih kolorimetrijskih metoda i omogućava vam da pronađete koncentraciju C x s greškom od 10-20%.
U ovom radu opisane su metode za analizu prirodnih voda na sadržaj različitih toksičnih supstanci, a u svim slučajevima se preporučuje metoda standardne skale. Međutim, po uputstvu nastavnika, analiza se može izvršiti i drugom vizuelnom metodom. Razmotrimo svojstva nekih toksičnih tvari koje se u prirodnim vodama mogu odrediti kolorimetrijskom metodom, kao i reakcije stvaranja obojenih spojeva iz njih. Upravo ove reakcije će se morati provesti u toku laboratorijskog rada.
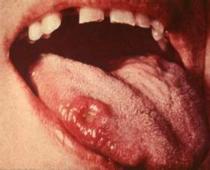
Određivanje fenola Fenoli su aromatična jedinjenja sa jednom ili više hidroksilnih grupa direktno vezanih za aromatično jezgro, kao što je benzenski prsten. U životnu sredinu ulaze iz otpadnih voda industrijskih preduzeća, posebno rafinerija koksa i nafte. Fenoli imaju snažno biološko dejstvo. Pri koncentraciji fenola od 0,50 mg/l u riječnoj vodi ribe uginu. U vodi za piće u Ruskoj Federaciji, maksimalno dozvoljena koncentracija fenola je 0,001 mg/l (u smislu najjednostavnijeg fenola C 6 H 5 OH). Sadržaj fenola u vodi za piće, prirodnim i otpadnim vodama kontrolišu laboratorije sanitarne službe i druge organizacije. Za određivanje fenola koriste se različite metode za njihovo pretvaranje u obojena jedinjenja; izbor metode analize zavisi od koncentracije fenola u ispitnoj vodi i prisutnosti interferirajućih supstanci. Ponekad se tokom analize količina fenola odvaja od nehlapljivih interferirajućih supstanci destilacijom fenola iz ispitnog uzorka vodenom parom, što u ovom radu nije potrebno. Ako se očekuje koncentracija fenola na nivou od 0,05-50 mg/l (jako zagađene vode), onda se analiza vrši po Griess metodi uz reakciju sa p-nitroanilinom. Ovaj reagens se dijazotira sa natrijum nitritom unapred (na dan analize), a zatim se vrši azo kuplovanje sa fenolom:
2H + ® + 2H 2 O
Rezultirajuća azo boja ima intenzivnu žuto-smeđu boju. Koncentracija boje će biti proporcionalna koncentraciji fenola u vodi ako se drugi reagensi (nitrit, p-nitroanilin) uzimaju u velikom i jednakom višku. Određivanje je neselektivno: različiti fenoli daju obojene proizvode sličnih svojstava. Prinos proizvoda u velikoj meri zavisi od pH vrednosti. Diazotizacija se vrši u kiseloj sredini, a azo kuplovanje u alkalnoj sredini.
Kada radite, imajte na umu da su fenoli i p-nitroanilin toksični. Pažljivo rukujte!
Određivanje nitrita Prisustvo povećane koncentracije nitrita u prirodnim vodama ukazuje da su one zagađene kućnim otpadnim vodama. Sadržaj nitrita u prirodnim vodama kreće se od nekoliko mikrograma do desetinki mg po 1 l (nitriti su manje toksični od fenola, MPC je 1 mg/l). Za određivanje nitrita, najčešće korištena kolorimetrijska metoda temelji se na reakciji nitrita sa sulfanilnom kiselinom i a-naftilaminom (Griess-Ilosvayeva reakcija). Prvo, prisutni nitriti reaguju sa sulfanilnom kiselinom (reakcija diazotizacije), zatim diazotizovana sulfanilna kiselina reaguje sa a-naftilaminom (reakcija azo kuplovanja), i nastaje crveno-ljubičasta boja:
Budući da se oba reagensa unose u velikom višku u odnosu na nitrite, koncentracija boje i optička gustoća njene otopine ovise samo o koncentraciji nitrita. Pivski zakon općenito vrijedi. Granica detekcije nitrita bez dodatne koncentracije je 1 mg/l. Jaka oksidaciona i redukciona sredstva ometaju.
Određivanje hlora Sadržaj "aktivnog hlora" se utvrđuje analizom hlorisane vode iz slavine. Otopljeni klor se također određuje u nekim otpadnim vodama, MPC C l = 0,4 mg / l. Osim molekula Cl 2, pojam "aktivnog hlora" uključuje i niz drugih nestabilnih jedinjenja hlora nastalih tokom hlorisanja vode, na primer hipohlorite, hloramine, itd. Sva ova jedinjenja reaguju kao slobodni hlor i određuju se ukupno . Rezultat analize je izražen u Cl 2 (mg/l). Određivanje treba izvršiti odmah nakon uzorkovanja vode.
Za određivanje malih količina hlora najpogodnija je kolorimetrijska metoda s o-toluidinom. Ovaj reagens se oksidira hlorom (kao i drugim oksidantima) mehanizmom koji nije u potpunosti razjašnjen, a otopina postaje žuta ili narančasta. Gvožđe (>0,3 mg/l) i nitriti (>0,1 mg/l) ometaju određivanje. U prisustvu brojnih ometajućih supstanci, određivanje hlora je ozbiljno komplikovano. Odgovarajuće tehnike opisane su u literaturi.
Budući da je standardna vaga koja sadrži oksidirani o-toluidin nestabilna tokom skladištenja, te je nepoželjno svakodnevno iznova pripremati, laboratorije često koriste stabilnu umjetnu vagu pripremljenu od otopina K 2 CrO 4 i K 2 Cr 2 O 7 . Boja standardnih otopina ove skale odgovara oku tačno kao boja otopina koje sadrže različite poznate količine produkta reakcije hlora sa o-toluidinom. Takve umjetne vage se u praksi često koriste.
Kolorimetrija kao metoda kemijske analize koristi se za određivanje koncentracije određene tvari u otopini. Metoda vam omogućava da radite s obojenim otopinama ili otopinama koje se mogu učiniti obojenim kao rezultat određene kemijske reakcije.
Osnove kolorimetrije
Metode hemijske analize pomoću kolorimetrije zasnovane su na Bouguer-Lambert-Veer zakonu, koji kaže da intenzitet boje zavisi od koncentracije obojene supstance u rastvoru i od debljine sloja tečnosti.
Koristeći različite kolorimetrijske tehnike, moguće je procijeniti kvantitativni sadržaj određenih tvari u otopini s prilično visokom preciznošću - obično je 0,1-1%. Ova tačnost, po pravilu, nije niža od preciznosti kojom se koncentracije određuju kao rezultat mnogo složenijih i skupljih hemijskih analiza, i dovoljna je za mnoge zadatke – ne samo industrijske, već i stručne. Kolorimetrijskim metodama se može odrediti koncentracija tvari do 10−8 mol/l.
Kolorimetrijske metode koriste vizuelno poređenje ili poređenje pomoću instrumenata - fotokolorimetara ili spektrofotometara. Poređenje se vrši direktnim ili kompenzacijskim metodama.
direktna metoda
 Direktna metoda uključuje poređenje stepena obojenosti ispitnog rastvora na određenoj temperaturi iu određenom sloju tečnosti sa referentnim rastvorom. Standard sadrži tačno poznatu količinu boje na istoj temperaturi i u istom sloju tečnosti.
Direktna metoda uključuje poređenje stepena obojenosti ispitnog rastvora na određenoj temperaturi iu određenom sloju tečnosti sa referentnim rastvorom. Standard sadrži tačno poznatu količinu boje na istoj temperaturi i u istom sloju tečnosti.
Ponekad se pravi poređenje sa destilovanom vodom. U pravilu se takve metode oslanjaju na upotrebu fotokolorimetara ili spektrofotometara. Ovi uređaji mjere jačinu struje u zavisnosti od intenziteta emitovane svjetlosti koja prolazi kroz ispitni rastvor.
Tačnost hardverskog mjerenja je veća od vizualne. Vizuelna metoda se također koristi za upoređivanje intenziteta boje otopine sa referentnim otopinama, čija je koncentracija tvari poznata.
Metod kompenzacije
Metoda kompenzacije zasniva se na dovođenju boje ispitnog uzorka na referentnu. Rješenja, koristeći različite optičke uređaje - ogledala, stakla i prizme, postavljaju se u uređaj na način da se kombinuju u vidnom polju istraživača. Oko je sposobno da fiksira istu boju dva uzorka sa velikom preciznošću. Kod nekih uređaja zadatak je olakšan činjenicom da kada se intenzitet boje poklopi, vizualna granica koja u početku razdvaja rješenja nestaje.
Da bi se proučavano rješenje dovelo do referentnog, u njega se dodaje prozirni rastvarač ili se povećava visina sloja tekućine. Zatim se iz vrijednosti dodanog razrjeđivača ili visine sloja otopine izvodi kvantitativna karakteristika koncentracije bojila u otopini. Metode kompenzacije koriste se u vizualnim kolorimetrima i fotokolorimetrima. Oni su najpraktičniji, jer na njih ne utječu vanjski faktori - na primjer, temperatura.
Kada i gdje se primjenjuju kolorimetrijske metode?
Kolorimetrijske metode za hemijsku analizu koriste se u slučajevima kada je poznat tačan hemijski sastav rastvora; rastvor je transparentan; postoji referentni uzorak; temperature uzorka i ispitnog rastvora su jednake. Pomoću ovih metoda moguće je odrediti koncentraciju supstanci u neobojenim otopinama, ako je moguće učiniti otopinu obojenom dodavanjem određenog reagensa.
Kolorimetrija se koristi:
U analitičkoj hemiji;
- u medicini (sadržaj krvi);
- vrši kontrolu kvaliteta vode za piće i otpadnih voda;
- u prehrambenoj industriji za određivanje stepena prečišćavanja vina, piva, šećera;
- u industriji - za analizu sastava ulja za podmazivanje, kerozina.
Prednosti kolorimetrijskih metoda:
Jednostavnost;
- nema potrebe za skupom opremom;
- efikasnost mjerenja, mogućnost izvođenja analiza direktno na proizvodnji;
- mogućnost određivanja vrlo malih koncentracija supstanci koje je teško izračunati drugim metodama hemijske analize.
U prodavnici laboratorijskog stakla i hemijske opreme "PrimeChemicalsGroup" možete kupiti i kolorimetrijske epruvete raznih veličina po pristupačnim cijenama. Vršimo dostavu širom Moskve i Moskovske regije.
- U kontaktu sa 0
- Google+ 0
- uredu 0
- Facebook 0