Ουσίες ανάλογα με την χρωματική ένταση των διαλυμάτων (ακριβέστερα, σύμφωνα με την απορρόφηση του φωτός από τα διαλύματα).
Βασικές πληροφορίες
Ένα από τα πρώτα χρωματόμετρα, που δημιουργήθηκε από τον Γάλλο οπτικό Jules Dubosque, 1880.
Η χρωματομετρία είναι μια μέθοδος για τον ποσοτικό προσδιορισμό της περιεκτικότητας ουσιών σε διαλύματα, είτε οπτικά είτε με τη χρήση οργάνων όπως τα χρωματόμετρα.
Η χρωματομετρία μπορεί να χρησιμοποιηθεί για την ποσοτικοποίηση όλων εκείνων των ουσιών που δίνουν έγχρωμα διαλύματα ή μπορεί, μέσω μιας χημικής αντίδρασης, να δώσει μια έγχρωμη διαλυτή ένωση. Οι χρωματομετρικές μέθοδοι βασίζονται στη σύγκριση της χρωματικής έντασης του διαλύματος δοκιμής, που μελετήθηκε στο εκπεμπόμενο φως, με το χρώμα ενός διαλύματος αναφοράς που περιέχει μια αυστηρά καθορισμένη ποσότητα της ίδιας έγχρωμης ουσίας ή με απεσταγμένο νερό.
Η ιστορία της εμφάνισης της χρωματομετρίας και της φωτομετρίας είναι περίεργη. Ο Yu. A. Zolotov αναφέρει ότι ο Robert Boyle (όπως και ορισμένοι επιστήμονες πριν από αυτόν) χρησιμοποίησε ένα εκχύλισμα τανινών για να διακρίνει μεταξύ του σιδήρου και του χαλκού σε διάλυμα. Ωστόσο, προφανώς, ήταν ο Boyle που παρατήρησε πρώτος ότι όσο περισσότερος σίδηρος περιέχεται στο διάλυμα, τόσο πιο έντονο είναι το χρώμα του τελευταίου. Αυτό ήταν το πρώτο βήμα προς τη χρωματομετρία. Και το πρώτο όργανο χρωματομετρίας ήταν το χρωματόμετρο τύπου Dubosque (1870), το οποίο χρησιμοποιούνταν μέχρι πρόσφατα.
Τα φωτοχρωμόμετρα και τα φασματοφωτόμετρα μετρούν την ποσότητα φωτός που μεταδίδεται σε ένα συγκεκριμένο μήκος κύματος φωτός. Ένας έλεγχος (συνήθως απεσταγμένο νερό ή πρώτη ύλη χωρίς πρόσθετα αντιδραστήρια) χρησιμοποιείται για τη βαθμονόμηση της συσκευής.
Η χρωματομετρία χρησιμοποιείται ευρέως στην αναλυτική χημεία, συμπεριλαμβανομένης της υδροχημικής ανάλυσης, ιδιαίτερα για την ποσοτική ανάλυση της περιεκτικότητας σε θρεπτικά συστατικά στα φυσικά νερά, για μέτρηση, στην ιατρική, καθώς και στη βιομηχανία για τον ποιοτικό έλεγχο των προϊόντων.
Φωτοχρωμομετρία
Φωτοχρωμομετρία- ποσοτικός προσδιορισμός της συγκέντρωσης μιας ουσίας με την απορρόφηση φωτός στις ορατές και σχεδόν υπεριώδεις περιοχές του φάσματος. Η απορρόφηση φωτός μετριέται με φωτοχρωμόμετρα ή φασματοφωτόμετρα.
Σημειώσεις
Ίδρυμα Wikimedia. 2010 .
Δείτε τι είναι η "Χρωματομετρία (χημική μέθοδος)" σε άλλα λεξικά:
Δεν πρέπει να συγχέεται με τη θερμιδομετρία. Χρωματομετρία (από το λατινικό χρώμα χρώμα και τα ελληνικά μετρεω μετρώ): Η χρωματομετρία (επιστήμη) είναι η επιστήμη της μέτρησης του χρώματος. Χρωματομετρία (χημική μέθοδος) μέθοδος χημικής ανάλυσης ... Wikipedia
Μελετά τη σχέση μεταξύ της σύνθεσης και των μακροσκοπικών ιδιοτήτων. συστήματα που αποτελούνται από πολλά πηγή σε σε (συστατικά). Για το F. x. ένα. Χαρακτηριστική είναι η αναπαράσταση αυτών των εξαρτήσεων γραφικά, με τη μορφή διαγράμματος, η σύνθεση της ιδιότητας. χρησιμοποιούνται και τραπέζια ...... Χημική Εγκυκλοπαίδεια
Περιεχόμενα ... Wikipedia
Αυτός ο όρος έχει άλλες έννοιες, βλέπε Χημεία (έννοιες). Χημεία (από το αραβικό کیمياء, που προέρχεται πιθανώς από την αιγυπτιακή λέξη km.t (μαύρο), από όπου το όνομα της Αιγύπτου, μαύρο χώμα και μόλυβδος «μαύρο ... ... Wikipedia
Το Βικιλεξικό έχει ένα άρθρο για την "οργανική χημεία"
Αυτός ο όρος έχει άλλες έννοιες, βλέπε Βιοχημεία (έννοιες). Η βιοχημεία (βιολογική ή φυσιολογική χημεία) είναι η επιστήμη της χημικής σύνθεσης των ζωντανών κυττάρων και των οργανισμών και των χημικών διεργασιών που αποτελούν τη βάση της δραστηριότητας της ζωής τους. ... ... Wikipedia
- (από άλλα ελληνικά γῆ «Γη» και από λόγος «διδασκαλία») η επιστήμη της σύνθεσης, της δομής και των προτύπων ανάπτυξης της Γης, άλλων πλανητών του ηλιακού συστήματος και των φυσικών δορυφόρων τους. Περιεχόμενα 1 Ιστορία της Γεωλογίας ... Wikipedia
Η κοινωνική εργασία είναι μια επαγγελματική δραστηριότητα για την οργάνωση βοήθειας και αλληλοβοήθειας ατόμων και ομάδων σε δύσκολες καταστάσεις ζωής, την ψυχοκοινωνική αποκατάσταση και ενσωμάτωσή τους. Στην πιο γενική του μορφή, η κοινωνική εργασία αντιπροσωπεύει τη ... ... Wikipedia
Γενικοί Όροι- Όροι της ρουμπρίκας: Γενικοί όροι Απόλυτα μαύρο σώμα Απόλυτο ελάχιστο Απόλυτος δείκτης χρήσης πόρων και εξοικονόμησης πόρων ... Εγκυκλοπαίδεια όρων, ορισμών και επεξηγήσεων δομικών υλικών
Αυτό το άρθρο ή ενότητα χρειάζεται αναθεώρηση. Βελτιώστε το άρθρο σύμφωνα με τους κανόνες για τη σύνταξη άρθρων. Η κβαντική χημεία είναι η κατεύθυνση ... Wikipedia
Η χρωματομετρία είναι μια από τις απλούστερες μεθόδους ανάλυσης απορρόφησης. Βασίζεται στην αλλαγή των χρωματικών αποχρώσεων του διαλύματος δοκιμής ανάλογα με τη συγκέντρωση. Οι χρωματομετρικές μέθοδοι μπορούν να χωριστούν σε οπτική χρωματομετρίακαι φωτοχρωματομετρία.
οπτική χρωματομετρία
Πραγματοποιείται εις βάρος των τυπικών σειρών. Για να γίνει αυτό, το διάλυμα δοκιμής συγκρίνεται με ένα σύνολο τυπικών διαλυμάτων, τα οποία πρέπει να είναι πρόσφατα παρασκευασμένα και να διαφέρουν μεταξύ τους κατά τουλάχιστον 10-15%.
Για παράδειγμα, ο χρωματομετρικός προσδιορισμός του pH σύμφωνα με τον Alyamovsky βασίζεται στην ιδιότητα των δεικτών να αλλάζουν το χρώμα τους ανάλογα με τη συγκέντρωση των ιόντων υδρογόνου που υπάρχουν στο διάλυμα.
Η κλίμακα του οργάνου Alyamovsky είναι μια σειρά από σφραγισμένους δοκιμαστικούς σωλήνες γεμάτους με έγχρωμο διάλυμα. Αυτό το φωτοσταθερό διάλυμα μιμείται το χρώμα ενός γενικού δείκτη σε συγκεκριμένο pH. Το διάλυμα δοκιμής συγκρίνεται με την κλίμακα και βρίσκεται ένας δοκιμαστικός σωλήνας σε αυτό που ταιριάζει περισσότερο σε χρώμα. Εάν το χρώμα του υγρού δεν ταιριάζει με το χρώμα των διαλυμάτων κλίμακας, τότε λάβετε τη μέση τιμή μεταξύ δύο δοκιμαστικών σωλήνων που πλησιάζουν σε χρώμα. Μερικές φορές μπορεί να υπάρχει ένα σύνολο Alyamovsky, στο οποίο η τυπική χρωματική κλίμακα δεν αντιπροσωπεύεται από αμπούλες με διαλύματα, αλλά από γυάλινες πλάκες με έγχρωμες μεμβράνες.
Για ευκολία σύγκρισης, προσαρτάται ένας συγκριτής στη συσκευή, αλλά η τεχνική σύγκρισης λύσεων με κλίμακα είναι διαφορετική σε αυτή την περίπτωση. Ο δοκιμαστικός σωλήνας με το έγχρωμο δοκιμαστικό διάλυμα πρέπει να τοποθετηθεί στην αριστερή υποδοχή του συγκριτή. Ρίξτε 5 ml απεσταγμένου νερού στον δοκιμαστικό σωλήνα από τη δεξιά υποδοχή του συγκριτή. Μια τυπική χρωματική κλίμακα εισάγεται στις υποδοχές του συγκριτή, ενώ το χρωματιστό τμήμα του θα πρέπει να είναι απέναντι στον δοκιμαστικό σωλήνα με απεσταγμένο νερό και το άχρωμο μέρος θα πρέπει να είναι στο δοκιμαστικό διάλυμα. Ο συγκριτής λαμβάνεται με το αριστερό χέρι και ανυψώνεται στο ύψος των ματιών, κρατώντας τη ζυγαριά μακριά σας και στρέφοντάς την προς το φως. Μετακινώντας την τυπική κλίμακα πάνω-κάτω, βρείτε το τμήμα της που ταιριάζει με το χρώμα του διαλύματος δοκιμής. Γυρνώντας τον συγκριτή με την κλίμακα προς το μέρος σας, μετρήστε την τιμή του pH και καταγράψτε το αποτέλεσμα της ανάλυσης.
Φωτοχρωμομετρία
Οι φωτοχρωματομετρικές μέθοδοι είναι μία από τις ευρέως χρησιμοποιούμενες ποικιλίες οπτικής ανάλυσης απορρόφησης. Για ακριβέστερο προσδιορισμό του αναλυόμενου στοιχείου, χρησιμοποιούνται ειδικές συσκευές - φωτοηλεκτροχρωμόμετρα (FEC).
Κατά την εργασία σε FEC, χρησιμοποιείται συχνότερα η μέθοδος της καμπύλης βαθμονόμησης, η οποία βασίζεται στην κατασκευή γραφήματος βαθμονόμησης στους άξονες "οπτική πυκνότητα - συγκέντρωση" για τυπικά διαλύματα γνωστής συγκέντρωσης. Με τη μέτρηση της οπτικής πυκνότητας του αναλυόμενου διαλύματος, η συγκέντρωσή του βρίσκεται από το γράφημα. Για καλύτερη αφομοίωση της φωτοχρωματομετρικής μεθόδου, οι μαθητές καλούνται να πραγματοποιήσουν εργαστηριακή ανάλυση του προσδιορισμού των ιόντων χαλκού και νικελίου σε διάλυμα με αυτή τη μέθοδο στο KFK-3-01.
Εργαστήριο 1
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΙΟΝΤΩΝ ΒΑΡΕΩΝ ΜΕΤΑΛΛΩΝ ΣΕ ΔΙΑΛΥΜΑ ΜΕ ΤΗ ΦΩΤΟΧΡΩΜΟΡΙΜΕΤΡΙΚΗ ΜΕΘΟΔΟ
Σκοπός:θα μάθει να εργάζεται στο φωτοχρωματόμετρο KFK-3-01. Προσδιορίστε την περιεκτικότητα σε ιόντα βαρέων μετάλλων στο KFK-3-01.
Η σειρά εργασίας στο φωτόμετρο KFK-3-01.
Κλείστε το καπάκι του διαμερίσματος της κυβέτας. Ενεργοποιήστε τον διακόπτη εναλλαγής "Δίκτυο". Μετά από 30 λεπτά, ξεκινήστε τη δουλειά. Ρυθμίστε το επιθυμητό μήκος κύματος.
- 1. Η ρύθμιση των μηκών κύματος πρέπει να γίνεται με σύνδεση από την πλευρά των μικρών μηκών κύματος σε μεγαλύτερα. Εάν, κατά την εγκατάσταση, η τιμή του μήκους κύματος υπερέβη την απαιτούμενη, είναι απαραίτητο να επιστρέψετε ξανά κατά 20-30 Nm σε μικρότερα κύματα και να ρυθμίσετε ξανά την επιθυμητή τιμή.
- 2. Πάρτε δύο κυβέτες. Ρίξτε απεσταγμένο νερό στο ένα και το διάλυμα δοκιμής στο άλλο. Οι κυβέτες γεμίζονται μέχρι το σημάδι στο πλάι. Δεν πρέπει να υπάρχουν σταγόνες στην εξωτερική επιφάνεια της κυβέτας.
- 3. Τοποθετήστε τις κυβέτες στο διαμέρισμα των κυττάρων. Τοποθετήστε την κυψελίδα με το «κενό δείγμα» στην μακρινή υποδοχή της θήκης της κυβέτας. Ρυθμίστε τη λαβή κίνησης της κυβέτας στην άκρα αριστερή θέση. Κλείστε το καπάκι του διαμερίσματος της κυβέτας.
- 4. Χρησιμοποιήστε το πλήκτρο "D" ή "C" για να επιλέξετε τη λειτουργία μέτρησης. Πατήστε το πλήκτρο "#". Στην κάτω ένδειξη, στην επάνω γραμμή, θα αναγράφεται "Graduation" μετά από 3-5 δευτερόλεπτα. Η επιγραφή θα εξαφανιστεί και θα εμφανιστεί "Αλλαγή" και το αποτέλεσμα της μέτρησης θα εμφανιστεί στην κάτω γραμμή. Ρυθμίστε το κουμπί κίνησης της κυβέτας προς τα δεξιά. Το αποτέλεσμα της μέτρησης (οπτική πυκνότητα του διαλύματος δοκιμής) θα εμφανιστεί στην κάτω γραμμή.
Εργασία 1. Προσδιορισμός της περιεκτικότητας σε C++ σε διάλυμα με φωτοχρωματομετρική μέθοδο.
Εξοπλισμός και αντιδραστήρια:φωτόμετρο KFK-3-01, κυψελίδα 3 cm, ογκομετρικές φιάλες 50 ml, πιπέτες 5,10 ml, πρότυπο διάλυμα Cu ++ - 0,5 mg/ml, διάλυμα αμμωνίας 1:1.
Πειραματική τεχνική
1. Επιλογή μήκους κύματος.
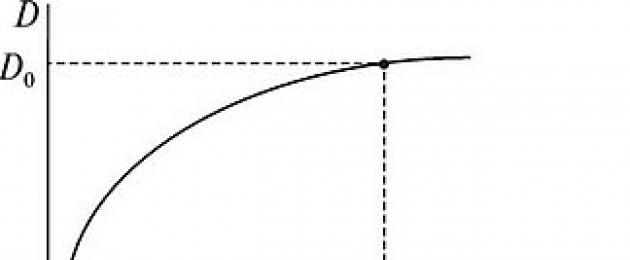
Σε ογκομετρική φιάλη των 50 ml, προσθέστε 14 ml πρότυπου διαλύματος Cu +2, προσθέστε 15 ml αμμωνίας και αραιώστε μέχρι τη χαραγή με νερό. Αναμίξτε και μετρήστε την οπτική πυκνότητα του διαλύματος /) από το μήκος κύματος Χ.Γέμισε το τραπέζι. 1. Αυτό το μήκος κύματος λαμβάνεται ως βέλτιστο X 0,στην οποία η τιμή της οπτικής πυκνότητας είναι μέγιστη για μια δεδομένη λύση (Εικ. 1).
Ρύζι. 1. Εξάρτηση οπτικής πυκνότητας μιστο μήκος κύματος Χ
2.
Σε ογκομετρικές φιάλες χωρητικότητας 50 ml, παρασκευάστε 5-6 διαλύματα Cu - ^ με διαφορετική περιεκτικότητα από 1 έως 7 mg / ml. Ο όγκος κάθε διαλύματος είναι 15 ml. Προσθέστε 15 ml αμμωνίας σε κάθε φιάλη και αραιώστε μέχρι τη χαραγή με νερό. Αναμείξτε και μετρήστε την οπτική πυκνότητα Καιστο επιλεγμένο μήκος κύματος Χ 0 .Γέμισε το τραπέζι. 2 και σχεδιάστε την εξάρτηση της οπτικής πυκνότητας;) από τη συγκέντρωση του διαλύματος C (Εικ. 2).

3. Προσδιορισμός της περιεκτικότητας σε Cu +2 στο διάλυμα ελέγχου.
Προσθέστε 10 ml νερού, 15 ml αμμωνίας στη φιάλη με διάλυμα ελέγχου. Φέρνουμε στο σημάδι με νερό και ανακατεύουμε. Μετρήστε την οπτική πυκνότητα του διαλύματος. Σύμφωνα με το γράφημα βαθμονόμησης (Εικ. 2), προσδιορίστε το C 0 - την περιεκτικότητα σε Cu +2 στο διάλυμα.
4. Βγάλτε συμπεράσματα από την εργασία.
Εργασία 2. Προσδιορισμός περιεκτικότητας Na+2 σε διάλυμα με φωτοχρωματομετρική μέθοδο.
Εξοπλισμός και αντιδραστήρια:φωτόμετρο KFK-3-01, κυψελίδα 3 cm, ογκομετρικές φιάλες 50 ml, σιφώνια 5,10 ml, πρότυπο διάλυμα 1Ch1 ++ - 0,01 mg/ml, διάλυμα αλκοόλης 1% διμεθυλγλυοξίμης, ιωδόνερο, διάλυμα αμμωνίας 1 :one.
Πειραματική τεχνική
1. Επιλογή μήκους κύματος.
Σε ογκομετρική φιάλη των 50 ml προσθέστε 10 ml πρότυπου διαλύματος αρ. , προσθέστε 5 ml ιωδιούχου νερού, 6 ml αμμωνίας και 2 ml διμεθυλογλυκοξίμης. Αραιώστε μέχρι το σημάδι με νερό, ανακατέψτε. Μετά από 5-7 λεπτά, μετρήστε την οπτική πυκνότητα του διαλύματος σε διαφορετικά μήκη κύματος. Γέμισε το τραπέζι. 1. Σχεδιάστε την εξάρτηση της οπτικής πυκνότητας του διαλύματος;> από το μήκος κύματος Χ.Το μήκος κύματος 7,0 στο οποίο η τιμή της οπτικής πυκνότητας είναι μέγιστη για μια δεδομένη λύση θεωρείται βέλτιστο (βλ. Εικ. 1).
2. Κατασκευή γραφήματος βαθμονόμησης.
Σε ογκομετρικές φιάλες χωρητικότητας 50 ml παρασκευάζονται 5-6 διαλύματα Νο +2 με διαφορετική περιεκτικότητα από 0,01 έως 0,1 mg/ml. Ο όγκος κάθε διαλύματος είναι 10 ml. Στη συνέχεια, προσθέστε αντιδραστήρια σε κάθε φιάλη, όπως υποδεικνύεται στην παράγραφο 1. Φέρτε τη χαραγή με νερό, ανακατέψτε. Μετά από 5-7 λεπτά, μετρήστε την οπτική πυκνότητα του διαλύματος στο επιλεγμένο μήκος κύματος. Γέμισε το τραπέζι. 2 και σχεδιάστε την εξάρτηση της οπτικής πυκνότητας Οστη συγκέντρωση του διαλύματος Γ (βλ. Εικ. 2).
3. Ορισμός περιεχομένου № +2 σε διάλυμα ελέγχου.
Προσθέστε 10 ml νερού στη φιάλη με το διάλυμα ελέγχου και στη συνέχεια προσθέστε τα αντιδραστήρια όπως υποδεικνύεται στην παράγραφο 1. Μετρήστε /) 0 - την οπτική πυκνότητα του διαλύματος. Σύμφωνα με το γράφημα βαθμονόμησης (Εικ. 3) C (), προσδιορίστε το C 0 - την περιεκτικότητα του Νο. +2 στο διάλυμα.
4. Εξάγετε συμπεράσματα για την εργασία.
Τραπέζι 1
(Filin V.A.Βιντεοοικολογία. Τι είναι καλό για τα μάτια και τι είναι κακό. Μ.: Videoekologiya, 1997).
Οι μέθοδοι ανάλυσης που βασίζονται στη σύγκριση της χρωματικής έντασης του διαλύματος δοκιμής και ενός διαλύματος ορισμένης συγκέντρωσης - τυπικής, ονομάζονται χρωματομετρικές (χρωματομετρία). Γίνεται διάκριση μεταξύ της οπτικής χρωματομετρίας, που πραγματοποιείται με τη βοήθεια του ματιού του παρατηρητή, και της φωτοηλεκτρικής χρωματομετρίας, που πραγματοποιείται με τη βοήθεια ενός φωτοκυττάρου.
Εάν μια δέσμη φωτός με ένταση I0 περάσει μέσα από το στρώμα διαλύματος, τότε αφού περάσει από αυτό το στρώμα η ένταση φωτός θα μειωθεί σε Αυτό. Η εξίσωση του βασικού νόμου της χρωματομετρίας - ο νόμος Bouguer-Lambert-Beer - έχει την ακόλουθη μορφή:
![]()
όπου Είναι η ένταση της φωτεινής ροής μετά τη διέλευση από το διάλυμα με συγκέντρωση C και πάχος στρώσης l. I0 - ένταση της προσπίπτουσας φωτεινής ροής. g είναι ένας συντελεστής που εξαρτάται από το μήκος κύματος του προσπίπτοντος φωτός, τη φύση της διαλυμένης ουσίας και τη θερμοκρασία του διαλύματος. ο συντελεστής g ονομάζεται συντελεστής μοριακής απόσβεσης. Ο λόγος της έντασης της φωτεινής ροής που διέρχεται από το διάλυμα It προς την ένταση της προσπίπτουσας φωτεινής ροής I0 ονομάζεται μετάδοση ή διαφάνεια και συμβολίζεται με το γράμμα T:

Η τιμή του Τ, που αναφέρεται σε πάχος στρώσης 1 cm, ονομάζεται διαπερατότητα. Ο λογάριθμος της αμοιβαίας μετάδοσης ονομάζεται εξάλειψη (εξάλειψη) E, ή οπτική πυκνότητα D:

Επομένως, η αποπληρωμή Ε είναι ευθέως ανάλογη με τη συγκέντρωση της ουσίας στο διάλυμα. Εάν απεικονίσουμε γραφικά την εξάρτηση της αποπληρωμής από τη συγκέντρωση, σχεδιάζοντας τη συγκέντρωση κατά μήκος της τετμημένης και την αποπληρωμή κατά μήκος της τεταγμένης, θα λάβουμε μια ευθεία γραμμή που εκτείνεται από την αρχή (Εικ. 52).

Ένα τέτοιο γράφημα καθιστά δυνατή την εξαγωγή συμπερασμάτων σχετικά με τη δυνατότητα εφαρμογής του βασικού νόμου της χρωματομετρίας στις λύσεις που μελετήθηκαν. Εάν η λύση υπακούει σε αυτόν τον νόμο, τότε το γράφημα που εκφράζει την εξάρτηση της αποπληρωμής. από τη συγκέντρωση, θα αντιπροσωπεύεται από μια ευθεία γραμμή. Εάν η λύση δεν υπακούει σε αυτόν τον νόμο, τότε η ευθύτητα παραβιάζεται σε κάποιο σημείο της καμπύλης ή σε όλο το μήκος της.
Μέθοδοι οπτικής χρωματομετρίας
Η οπτική χρωματομετρία πραγματοποιείται σύμφωνα με μία από τις ακόλουθες μεθόδους: 1) τυπική μέθοδος σειράς. 2) χρωματομετρική μέθοδος τιτλοδότησης ή διπλασιασμού. 3) μέθοδος εξισορρόπησης χρώματος. Τα δύο πρώτα από αυτά δεν απαιτούν συμμόρφωση με τον βασικό νόμο της χρωματομετρίας. η μέθοδος εξισορρόπησης χρώματος απαιτεί την υπαγωγή των λύσεων στον βασικό νόμο της χρωματομετρίας.

Τυπική μέθοδος σειράς
Η ουσία της μεθόδου.Όταν χρωματομετρείται με τη μέθοδο της τυπικής σειράς, το διάλυμα δοκιμής σε μια στρώση ορισμένου πάχους συγκρίνεται με ένα σύνολο τυπικών διαλυμάτων του ίδιου πάχους στρώσης, που διαφέρουν μεταξύ τους ως προς την ένταση χρώματος κατά περίπου 10-15%. Η άγνωστη συγκέντρωση είναι ίση με τη συγκέντρωση ενός τυπικού διαλύματος, το χρώμα του οποίου ταιριάζει με το χρώμα του διαλύματος δοκιμής ή είναι μεταξύ των δύο πλησιέστερων πιο αδύναμων ή πιο έντονα χρωματισμένων. Η τυπική μέθοδος σειράς μπορεί να χρησιμοποιηθεί για τον προσδιορισμό της περιεκτικότητας σε αλδεΰδες, πετρέλαιο fusel και μεθυλική αλκοόλη στην ανορθωμένη αλκοόλη. Το χρώμα συγκρίνεται σε δοκιμαστικούς σωλήνες με εδαφισμένα πώματα ίδιας διαμέτρου κατασκευασμένα από άχρωμο γυαλί ίδιου πάχους. Οι χρωματομετρικοί δοκιμαστικοί σωλήνες τοποθετούνται σε ειδική βάση (Εικ. 53) και σε φόντο παγωμένου γυαλιού ή φύλλου λευκού χαρτιού, το χρώμα του δοκιμαστικού διαλύματος συγκρίνεται με το χρώμα των τυπικών διαλυμάτων. Όταν χρησιμοποιείτε σωλήνες με επίπεδο πυθμένα, τα χρώματα μπορούν να συγκριθούν κοιτάζοντας τις λύσεις από πάνω. Αυτό είναι ιδιαίτερα χρήσιμο όταν εργάζεστε με ξυραφάκια ασθενούς χρώματος.
1) Πρότυπα διαλύματα ισοαμυλικής αλκοόλης με περιεκτικότητα 0,0005. 0,001; 0,002 και 0,003% vol. σε αιθανόλη 96% χωρίς fusel oil και αλδεΰδες.
2) Διάλυμα 0,05% παραδιμεθυλαμινοβενζαλδεΰδης σε πυκνό χ. συμπεριλαμβανομένου του θειικού οξέος με σχετική πυκνότητα 1.835.
Πρόοδος ανάλυσης. 0,5 ml της υπό δοκιμή αλκοόλης μετράται με βαθμονομημένη πιπέτα ανά 1 ml και τοποθετείται σε καθαρή, στεγνή φιάλη με επίπεδο πυθμένα με μακρύ λαιμό, όπου προστίθενται 10 ml διαλύματος παραδιμεθυλαμινοβενζαλδεΰδης από τον κύλινδρο μέτρησης. Το περιεχόμενο αναμειγνύεται, η φιάλη βυθίζεται σε λουτρό ζέοντος νερού και διατηρείται σε βραστό νερό για ακριβώς 20 λεπτά. Ένα γυάλινο ποτήρι ζέσεως 300 ml χρησιμοποιείται ως υδατόλουτρο. Ο λαιμός της φιάλης πρέπει να είναι σε κεκλιμένη θέση όταν βράζει. Μετά από 20 λεπτά, η φιάλη ψύχεται γρήγορα σε τρεχούμενο νερό. Ταυτόχρονα, το περιεχόμενο της φιάλης αποκτά ένα ανοιχτό κιτρινωπό-ροζ χρώμα, που μετατρέπεται σε ροζ ποικίλης έντασης, ανάλογα με την περιεκτικότητα σε λάδι καυσίμου.
Το περιεχόμενο της φιάλης χύνεται σε δοκιμαστικό σωλήνα με αλεσμένο πώμα. Το χρώμα της υπό δοκιμή αλκοόλης συγκρίνεται με το χρώμα των τυποποιημένων διαλυμάτων που έχουν υποβληθεί στην ίδια επεξεργασία με την υπό δοκιμή αλκοόλη. Κατά σύμπτωση των χρωμάτων, προσδιορίζεται η περιεκτικότητα σε λάδι καυσίμου στην αλκοόλη δοκιμής.
Χρωματομετρική μέθοδος τιτλοδότησης
Στη μέθοδο χρωματομετρικής τιτλοδότησης, ένας συγκεκριμένος όγκος έγχρωμου διαλύματος άγνωστης συγκέντρωσης προς δοκιμή συγκρίνεται με τον ίδιο όγκο νερού στον οποίο προστίθεται έγχρωμο πρότυπο διάλυμα συγκεκριμένης συγκέντρωσης. Προσθέστε το διάλυμα από την προχοΐδα (τιτλοδότηση) μέχρι το χρώμα να γίνει ίσο με το διάλυμα δοκιμής. Στον τεχνοχημικό έλεγχο των φυτών ζύμωσης, αυτή η μέθοδος χρησιμοποιείται για τον προσδιορισμό του χρώματος της μπύρας, το οποίο εκφράζεται σε χιλιοστόλιτρα 0,1 N. διάλυμα ιωδίου προστίθεται σε 100 ml απεσταγμένου νερού για να εξισορροπηθεί το χρώμα με 100 ml μπύρας. Πρόοδος. Αυτός ο ορισμός γίνεται ως εξής. Δύο πανομοιότυπα χημικά ποτήρια χωρητικότητας 150-200 ml τοποθετούνται σε ένα φύλλο λευκού χαρτιού ή σε ένα λευκό πορσελάνινο πιάτο. Στο ένα ρίχνουμε 100 ml μπύρας, στο άλλο 100 ml απεσταγμένο νερό. Σε ένα ποτήρι νερό χύνεται από προχοΐδα με ανάδευση 0,1 N. διάλυμα ιωδίου έως ότου το χρώμα των υγρών γίνει το ίδιο όταν το βλέπουμε από πάνω και από το πλάι (μέσα από το υγρό).
Μέθοδος εξισορρόπησης χρώματος
Φανταστείτε ότι υπάρχουν δύο έγχρωμα διαλύματα που περιέχουν την ίδια έγχρωμη ουσία, αλλά σε διαφορετικές συγκεντρώσεις. Η εξαργύρωση καθεμιάς από τις λύσεις θα είναι αντίστοιχα ίση με
Αλλάζοντας το πάχος του στρώματος αυτών των διαλυμάτων (l), είναι δυνατό να επιτευχθεί μια κατάσταση στην οποία, παρά τις διαφορετικές συγκεντρώσεις, η ένταση της ροής φωτός που διέρχεται και από τα δύο διαλύματα θα είναι η ίδια - θα έρθει η οπτική ισορροπία. Αυτό θα συμβεί όταν και τα δύο διαλύματα απορροφήσουν το ίδιο κλάσμα φωτός, δηλ. όταν οι αποπληρωμές των λύσεων θα είναι ίσες? σε αυτή την περίπτωση, E1 = E2 και eC1l1 = eC2l2. Ο συντελεστής απόσβεσης e και των δύο διαλυμάτων είναι ο ίδιος (το διάλυμα περιέχει την ίδια ουσία). Συνεπώς,
![]()

εκείνοι. τα πάχη των στρωμάτων των διαλυμάτων με το ίδιο παρατηρούμενο χρώμα είναι αντιστρόφως ανάλογα με τις συγκεντρώσεις των διαλυμάτων. Αυτή η σχέση μεταξύ του πάχους του στρώματος και της συγκέντρωσης είναι η βάση της μεθόδου εξισορρόπησης χρώματος.

Η εξίσωση των χρωμάτων πραγματοποιείται σε ειδικές συσκευές - χρωματόμετρα. Ένα πολύ κοινό χρωματόμετρο εμβάπτισης είναι το σύστημα Dubosque. Το οπτικό σχήμα αυτού του χρωματόμετρου έχει ως εξής (Εικ. 54). Η ροή φωτός από τον καθρέφτη 1 διέρχεται από το στρώμα του διαλύματος δοκιμής στο κελί 2, έμβολο 4, πρίσμα 6, φακοί 8 και 9 και εισέρχεται στον προσοφθάλμιο φακό, φωτίζοντας το δεξί μισό του οπτικού πεδίου. Μια άλλη ροή φωτός διέρχεται από το τυπικό στρώμα διαλύματος στο κελί 3, έμβολο 5, πρίσμα 7, φακούς 8 και 9 και εισέρχεται στον προσοφθάλμιο φακό, φωτίζοντας το αριστερό μισό του οπτικού πεδίου. Με την αλλαγή του ύψους των στηλών των διαλυμάτων με τη βοήθεια ενός rack, επιτυγχάνεται οπτική ισορροπία - η εξαφάνιση της διεπαφής. Η γενική άποψη του χρωματόμετρου φαίνεται στο σχ. 55.

Το χρώμα των αλκοολούχων ποτών καθορίζεται από ένα χρωματόμετρο, το οποίο είναι ένα χρωματόμετρο εμβάπτισης τύπου Dubosque, στο οποίο μία από τις κυβέτες αντικαθίσταται από ένα πλαίσιο στο οποίο τοποθετείται το αντίστοιχο πρότυπο ξηρού χρώματος. Τα πρότυπα συμπαγούς χρώματος είναι μια οξική μεμβράνη βαμμένη με μόνιμες χημικές βαφές.
Για τη μέτρηση του χρώματος του προϊόντος δοκιμής, μετά το φιλτράρισμα, χύνεται στην κυψελίδα 1 του μετρητή χρώματος (Εικ. 56) και το αντίστοιχο πρότυπο 2 τοποθετείται σε ειδική βάση. Ακτίνες φωτός, έχοντας περάσει την κυψελίδα με τη δοκιμή το διάλυμα και το χρωματικό πρότυπο, εισαγάγετε μέσα από τα πρίσματα 3 και 4 στον θάλαμο 5 με δύο πρίσματα που κατευθύνουν τις ακτίνες φωτός στο τηλεσκόπιο 6. Στο τηλεσκόπιο, παρατηρείται ένα πεδίο, το μισό του οποίου φωτίζεται από μια δέσμη που διέρχεται από προϊόν υπό μελέτη. Ο ομοιόμορφος χρωματισμός και των δύο τμημάτων του χωραφιού επιτυγχάνεται ανυψώνοντας ή χαμηλώνοντας την κυψελίδα 1 με τη βοήθεια μιας σχάρας.
Μετά την εξίσωση του χρώματος και στα δύο τμήματα του οπτικού πεδίου, το ύψος της στήλης υγρού σε χιλιοστά υπολογίζεται στην κλίμακα της συσκευής και συγκρίνεται με το ύψος της στήλης που έχει εγκριθεί για ένα δεδομένο προϊόν. Έτσι, για το λικέρ πορτοκαλιού, χρησιμοποιείται το πρότυπο Νο. 7, το ύψος της στήλης στην κλίμακα του μετρητή χρώματος πρέπει να είναι 33 mm, για το λικέρ σοκολάτας - πρότυπο Νο. 14, το ύψος της στήλης είναι 26 mm. Τα καθορισμένα δεδομένα για όλα τα αλκοολούχα προϊόντα δίνονται στις οδηγίες για τον τεχνικό και χημικό έλεγχο της παραγωγής αλκοολούχων ποτών. Εάν τα ληφθέντα στοιχεία είναι ίσα ή διαφέρουν μεταξύ τους κατά ±5, τότε θεωρείται ότι το χρώμα του προϊόντος δοκιμής αντιστοιχεί στο εγκεκριμένο δείγμα. Εάν το ύψος που προκύπτει είναι μεγαλύτερο από το εγκεκριμένο, το προϊόν είναι υποβαμμένο, αν είναι μικρότερο, τότε ξαναβάφεται.
Το σύνολο προτύπων περιέχει άχρωμα αντισταθμιστικά φίλτρα, τα οποία χρησιμοποιούνται για την εξίσωση της φυσικής φωτεινότητας των χρωμάτων ορισμένων προϊόντων με τη φωτεινότητα χρώματος του φίλτρου χρώματος. Ο αντισταθμιστής τοποθετείται στην φωτεινή οπή του χρωματόμετρου κάτω από την κυψελίδα με το προϊόν.
Φωτοχρωματομετρική μέθοδος
Η μέθοδος αυτή περιγράφεται στο κεφάλαιο του βιβλίου «Τεχνοχημικός έλεγχος ξήρανσης λαχανικών και παραγωγής συμπυκνώματος τροφίμων».
Χρωματομετρικός προσδιορισμός της περιεκτικότητας σε υδατάνθρακες σε ημιπροϊόντα παραγωγής αλκοόλης (μέθοδος VNIISL)
Το αντιδραστήριο για τον προσδιορισμό της περιεκτικότητας σε υδατάνθρακες με τη χρωματομετρική μέθοδο σε ημιπροϊόντα παραγωγής αλκοόλης είναι το διάλυμα ανθρόνης σε χημικό. συμπεριλαμβανομένου θειικού οξέος με σχετική πυκνότητα 1,830 (συγκέντρωση 0,2% κ.β.). Σε ένα έντονα όξινο περιβάλλον, η γλυκόζη αποσυντίθεται για να σχηματίσει παράγωγα φουρφουράλης, τα οποία αντιδρούν με την ανθρόνη για να σχηματίσουν μια πράσινη σύμπλοκη ένωση. Αυτή η μέθοδος καθορίζει τη συνολική ποσότητα υδατανθράκων και τα δεδομένα λαμβάνονται σε μονάδες γλυκόζης. Δεν απαιτείται προκαταρκτική υδρόλυση των πολυσακχαριτών σε γλυκόζη, καθώς η αντίδραση με την ανθρόνη προχωρά σε ένα έντονα όξινο περιβάλλον. Στην περίπτωση αυτή, οι πολυσακχαρίτες υδρολύονται σε μονοσακχαρίτες, οι οποίοι αντιδρούν με την ανθρόνη.

Για τον προσδιορισμό της περιεκτικότητας σε υδατάνθρακες, είναι απαραίτητο να κατασκευαστεί μια καμπύλη βαθμονόμησης σε διαλύματα x. συμπεριλαμβανομένης της γλυκόζης με συγκέντρωση 5-10 mg / 100 ml (Εικ. 59). Η καμπύλη βαθμονόμησης είναι κατασκευασμένη ως εξής. Προετοιμάστε διαλύματα x. συμπεριλαμβανομένης της γλυκόζης με συγκέντρωση 5 έως 10 mg σε 100 ml διαλύματος ανά χιλιοστόγραμμα. Στη συνέχεια, 5 ml του αντιδραστηρίου χύνονται σε δοκιμαστικό σωλήνα 20 ml από πυρίμαχο γυαλί και προστίθενται προσεκτικά εκεί 2,5 ml του παρασκευασμένου διαλύματος γλυκόζης, έτσι ώστε να σχηματιστούν δύο στοιβάδες. Ο σωλήνας κλείνεται με αλεσμένο πώμα, το περιεχόμενό του αναμιγνύεται γρήγορα και ο σωλήνας τοποθετείται σε λουτρό βραστό νερό για 6 λεπτά. Μετά από αυτό το χρονικό διάστημα, ο σωλήνας αφαιρείται από το λουτρό, το μείγμα της αντίδρασης ψύχεται στους 20 ° C και το έγχρωμο διάλυμα είναι χρωματομετρικό σε ένα φωτοχρωματόμετρο χρησιμοποιώντας ένα φίλτρο φωτός με μήκος κύματος φωτός 610 nm και μια κυψελίδα με μήκος προσώπου 5 mm. Οι μετρήσεις ξεκινούν με το πιο συμπυκνωμένο διάλυμα (σε αυτό το παράδειγμα, 10 mg γλυκόζης σε 100 ml διαλύματος). Η οπτική πυκνότητα μετριέται χρησιμοποιώντας το αριστερό τύμπανο. Έχοντας μετρήσει την οπτική πυκνότητα όλων των διαλυμάτων, δημιουργείται μια καμπύλη βαθμονόμησης, που απεικονίζει τις γνωστές συγκεντρώσεις κατά μήκος του άξονα της τετμημένης και τις αντίστοιχες οπτικές πυκνότητες κατά μήκος του άξονα των τεταγμένων. Όπως φαίνεται από την παραπάνω καμπύλη (βλ. Εικ. 59), η οπτική πυκνότητα αυξάνεται ανάλογα με τη συγκέντρωση της γλυκόζης στο διάλυμα. Αυτή η εξάρτηση εκφράζεται με μια ευθεία γραμμή.
Για τον προσδιορισμό των υδατανθράκων, το διάλυμα δοκιμής αραιώνεται σε περιεκτικότητα 5-10 mg σε 100 ml διαλύματος και ο προσδιορισμός πραγματοποιείται με αυτόν τον τρόπο: 5 ml του μείγματος της αντίδρασης χύνεται σε δοκιμαστικό σωλήνα και στη συνέχεια 2,5 ml από το Το δοκιμαστικό διάλυμα προστίθεται προσεκτικά έτσι ώστε να σχηματιστούν δύο στρώσεις. Στο μέλλον, προχωρήστε όπως στην κατασκευή της καμπύλης βαθμονόμησης. Έχοντας καθορίσει την οπτική πυκνότητα D κατά μήκος της γραμμής βαθμονόμησης, βρίσκεται η περιεκτικότητα σε γλυκόζη στο διάλυμα. Η περιεκτικότητα σε γλυκόζη σε ένα διάλυμα μπορεί επίσης να υπολογιστεί χρησιμοποιώντας την εξίσωση
![]()
που είναι η εξίσωση της γραμμής βαθμονόμησης και βασίζεται στις συντεταγμένες αυτής της γραμμής.
Τυπικά, η οπτική πυκνότητα προσδιορίζεται σε κυψελίδα με μήκος προσώπου 5 mm. Εάν το διάλυμα γλυκόζης είναι πολύ συμπυκνωμένο, τότε μετά την αντίδραση με ανθρόνο, θα ληφθεί ένα πολύ έντονα χρωματισμένο διάλυμα, η οπτική πυκνότητα του οποίου θα είναι μεγαλύτερη από την οριακή οπτική πυκνότητα του τυμπάνου του φωτοχρωματομέτρου και δεν θα είναι δυνατός ο προσδιορισμός του. αξία; με ένα πολύ αραιωμένο διάλυμα γλυκόζης, η τιμή της οπτικής πυκνότητας θα είναι μικρή και το σφάλμα στον προσδιορισμό είναι σημαντικό. Και στις δύο περιπτώσεις, η ανάλυση θα πρέπει να επαναληφθεί, αλλάζοντας ανάλογα την αραίωση του διαλύματος. Είναι επίσης δυνατό, χωρίς επανάληψη της ανάλυσης, να προσδιοριστεί η οπτική πυκνότητα χρησιμοποιώντας μια άλλη κυψελίδα κατά τη χρωματομετρία: για έντονα έγχρωμα διαλύματα με μήκος προσώπου 3 ή 1 mm, για διαλύματα ασθενούς χρώματος - 10 ή 20 mm. Έχοντας αποκτήσει την οπτική πυκνότητα σε άλλες κυψελίδες, είναι αδύνατο να προσδιοριστεί η περιεκτικότητα σε γλυκόζη χρησιμοποιώντας μια γραμμή βαθμονόμησης που έχει σχεδιαστεί σε σχέση με μια κυψελίδα με μήκος προσώπου 5 mm. Είναι απαραίτητο να υπολογιστεί πρώτα η τιμή της οπτικής πυκνότητας του διαλύματος, η οποία προκύπτει για αυτό το μήκος της άκρης της κυβέτας σύμφωνα με την εξίσωση

όπου D5 είναι η οπτική πυκνότητα του διαλύματος που λαμβάνεται με χρήση κυψελίδας μήκους προσώπου 5 mm. Dx είναι η οπτική πυκνότητα του διαλύματος που λαμβάνεται σε μια κυψελίδα με μήκος όψης 1 mm.
Αυτή η μέθοδος εφαρμόζεται σε διαλύματα που περιέχουν υπολείμματα γλυκόζης στα οποία δεν υπάρχουν πεντόζες και πεντοσάνες.
Προσδιορισμός της περιεκτικότητας σε διαλυτούς μη ζυμωμένους υδατάνθρακες σε ώριμο πολτό δημητριακών-πατάτας (μέθοδος VNIISL)
Ο ώριμος πουρές δημητριακών-πατάτας, μαζί με υδατάνθρακες που μπορούν να μετατραπούν σε αλκοόλ (άμυλο, δεξτρίνες, μαλτόζη, γλυκόζη), περιέχει επίσης πεντόζες και πεντοσάνες, οι οποίες δεν μετατρέπονται σε αλκοόλ. Όταν προσδιορίζεται με τη χημική μέθοδο, βρίσκεται η συνολική ποσότητα υδατανθράκων. Εν τω μεταξύ, είναι πολύ σημαντικό να γνωρίζουμε την περιεκτικότητα του πολτού σε ζυμώσιμους υδατάνθρακες, οι οποίοι θα μπορούσαν να ζυμωθούν, αλλά δεν ζυμώθηκαν λόγω ατελούς σακχαροποίησης και ζύμωσης - οι λεγόμενοι μη ζυμωμένοι υδατάνθρακες. Μέχρι πρόσφατα, καθορίζονταν από τη διαφορά μεταξύ της συνολικής ποσότητας υδατανθράκων και πεντόζων. ο προσδιορισμός των πεντόζων (βλ. σελ. 82) είναι συγκριτικά δύσκολος και χρονοβόρος. Η χρωματομετρική ανάλυση καθιστά δυνατό τον άμεσο προσδιορισμό των μη ζυμωθέντων υδατανθράκων στον πολτό.
Το Anthrone είναι γνωστό ότι λερώνει με όλους τους υδατάνθρακες, συμπεριλαμβανομένων των πεντόζων. Ωστόσο, η αντίδραση ανθρόνης είναι περίπου 12 φορές λιγότερο ευαίσθητη στον προσδιορισμό των πεντόζων από ό,τι στην ανάλυση των εξόζων. Η VNIISL έχει αναπτύξει μια νέα τροποποίηση της μεθόδου ανθρόνης, στην οποία εξαλείφεται η επίδραση των πεντόζων και των πεντοζανών στα αποτελέσματα της ανάλυσης. Αυτή η τροποποίηση βασίζεται στον ακόλουθο νόμο της χρωματομετρίας: η οπτική πυκνότητα ενός μείγματος συστατικών είναι ίση με το άθροισμα των γινομένων των συντελεστών απόσβεσης των επιμέρους συστατικών και της συγκέντρωσής τους
όπου D είναι η οπτική πυκνότητα του μείγματος, ίση με lg0/l. Εδώ l0 είναι η ένταση του αρχικού φωτός. l είναι η ένταση του φωτός που διέρχεται από το διάλυμα. e1, e2, ..., en - αναλογίες εξαγοράς;
Εδώ D είναι η οπτική πυκνότητα του συστατικού, C είναι η συγκέντρωση του συστατικού στο διάλυμα, l είναι το μήκος της επιφάνειας της κυβέτας.
Η οπτική πυκνότητα του διαλύματος εξαρτάται από το μήκος κύματος. Κατά την ανάπτυξη της μεθόδου, επιλέχθηκαν δύο κύματα. Με ένα από αυτά, το πρώτο συστατικό (γλυκόζη) έχει μια έντονη ζώνη και το δεύτερο (αραβινόζη) απορροφάται πολύ ασθενώς. Σε διαφορετικό μήκος κύματος, η εικόνα πρέπει να αντιστραφεί. Με βάση τις μελέτες που πραγματοποιήθηκαν, επιλέχθηκαν για χρωματομετρία φίλτρα φωτός με μήκος κύματος φωτός 610 και 413 nm.
Ο προσδιορισμός της περιεκτικότητας σε μη ζυμωμένους υδατάνθρακες στον πολτό πραγματοποιείται ως εξής. Ζυγίζεται μερίδα 25 g του διηθήματος πολτού σε ένα ποτήρι και μεταφέρεται σε ογκομετρική φιάλη των 200 ml. Το ποτήρι ξεπλένεται με νερό και τα πλυσίματα χύνονται στην ίδια φιάλη. Στη συνέχεια, 2 ml διαλύματος θειικού ψευδαργύρου 30% προστίθενται στη φιάλη για διαύγαση, αναδεύονται, διατηρούνται για 2-3 λεπτά και προστίθενται 2 ml διαλύματος 15% κίτρινου άλατος αίματος και αναμειγνύονται ξανά. Ο όγκος του διαλύματος αυξήθηκε μέχρι τη χαραγή με απεσταγμένο νερό.
Το διάλυμα διηθείται σε ξηρή φιάλη. Τα πρώτα 20-30 ml του διηθήματος απορρίπτονται και τα επόμενα τμήματα χρησιμοποιούνται για ανάλυση. Το διήθημα αραιώνεται για δεύτερη φορά έτσι ώστε 100 ml του διαλύματος να περιέχουν υδατάνθρακες από 5 έως 12 mg. Για προσδιορισμό, 10 ml αντιδραστηρίου ανθρόνης χύνονται σε δοκιμαστικό σωλήνα 20 ml με αλεσμένο πώμα και προστίθενται προσεκτικά 5 ml του διαλύματος δοκιμής, έτσι ώστε τα υγρά να μην αναμειγνύονται, αλλά να προκύπτουν δύο στρώσεις. ο σωλήνας κλείνεται με πώμα. Παράλληλα, παρασκευάστε ένα τυφλό διάλυμα προσθέτοντας 5 ml απεσταγμένου νερού σε 10 ml του αντιδραστηρίου. Τα περιεχόμενα των σωλήνων αναδεύονται ζωηρά για 10 δευτερόλεπτα και βυθίζονται σε υδατόλουτρο που βράζει έντονα. Ο βρασμός θα πρέπει να ξαναρχίσει εντός 0,5 λεπτού από τη στιγμή που οι σωλήνες βυθίζονται στο λουτρό. Παρατηρείται η έναρξη του βρασμού του νερού στο λουτρό και αφήνεται να παραμείνει για 5,5 λεπτά για να πραγματοποιηθεί η αντίδραση. Μετά τη γήρανση, οι σωλήνες ψύχονται σε λουτρό με τρεχούμενο νερό στους 20 ° C. Η οπτική πυκνότητα του προκύπτοντος διαλύματος προσδιορίζεται στο αριστερό τύμπανο του φωτοηλεκτρικού χρωματόμετρου χρησιμοποιώντας δύο φίλτρα φωτός: πορτοκαλί με μήκος κύματος L = 610 nm και μπλε-ιώδες με μήκος κύματος L = 413 nm σε κυβέτα με μήκος προσώπου 5 mm . Η κυψελίδα ξεπλένεται 2-3 φορές με το διάλυμα δοκιμής και στη συνέχεια γεμίζεται έτσι ώστε το υγρό να μην φτάσει στις άκρες κατά 5 mm. Τα εξωτερικά τοιχώματα της κυβέτας πλένονται με πίδακα νερού και σκουπίζονται με στεγνό διηθητικό χαρτί. Με τον ίδιο τρόπο, ένα τυφλό διάλυμα χύνεται σε δύο άλλες κυψελίδες ίδιου μεγέθους και προσδιορίζεται η οπτική πυκνότητα.
Σύμφωνα με τις τιμές της οπτικής πυκνότητας, η περιεκτικότητα σε διαλυτούς μη ζυμωμένους υδατάνθρακες βρίσκεται σύμφωνα με τις εξισώσεις:

Όπου D1 είναι η οπτική πυκνότητα με ένα φίλτρο φωτός με μήκος κύματος L = 610 nm. D2 - οπτική πυκνότητα με φίλτρο φωτός με μήκος κύματος L = 413 nm. n είναι ο συντελεστής αραίωσης.
Σύντομες θεωρητικές πληροφορίες Οι χρωματομετρικές μέθοδοι βασίζονται σε οπτική αξιολόγηση της απορρόφησης φωτός από διαλύματα. Η χρωματομετρική ανάλυση είναι ένα μικρό μέρος της φασματοφωτομετρικής ανάλυσης. Οι απλούστερες χρωματομετρικές μέθοδοι εμφανίστηκαν τον 19ο αιώνα (για παράδειγμα, μέθοδοι ανάλυσης μεταλλικών νερών), αλλά ακόμη και σήμερα σε αγροχημικές, υδροχημικές και κλινικές αναλύσεις, χρησιμοποιούνται εξπρές μέθοδοι που δεν απαιτούν όργανα και εργαστηριακό εξοπλισμό. Οι χρωματομετρικές μέθοδοι χρησιμοποιούνται όπου η ταχύτητα και το χαμηλό κόστος ανάλυσης είναι πιο σημαντικά από την ακρίβειά της. Σημειώστε ότι στις σύγχρονες χρωματομετρικές τεχνικές, χρησιμοποιούνται οι ίδιες φωτομετρικές αντιδράσεις όπως στις ενόργανες μεθόδους μέτρησης της απορρόφησης φωτός.
Μπορούν να χρησιμοποιηθούν διάφορες παραλλαγές χρωματομετρικής ανάλυσης για την εκτίμηση της συγκέντρωσης της αναλυόμενης ουσίας.
1. Τυπική μέθοδος κλίμακας.Αυτή είναι η πιο κοινή και ταχύτερη από όλες τις χρωματομετρικές μεθόδους. Σε αυτό, το ορατό χρώμα του διαλύματος δοκιμής συγκρίνεται σε πανομοιότυπους κυλίνδρους ή δοκιμαστικούς σωλήνες με μια σειρά από έγχρωμα διαλύματα της ίδιας σύνθεσης, αλλά με γνωστή περιεκτικότητα της αναλυόμενης ουσίας X. συγκέντρωση Χ στο διάλυμα δοκιμής, παρασκευάστε μια νέα, πιο λεπτομερής κλίμακα για αυτό το συγκεκριμένο εύρος συγκέντρωσης και στη συνέχεια να βελτιώσετε το αποτέλεσμα της ανάλυσης χρησιμοποιώντας το. Η τυπική μέθοδος κλίμακας δεν απαιτεί την τήρηση του νόμου της μπύρας (σε αντίθεση με τη μέθοδο προσαρμογής) και δίνει σφάλμα της τάξης του 30% rel.
Δεδομένου ότι το ανθρώπινο μάτι διακρίνει τις αποχρώσεις των χρωμάτων πολύ καλύτερα από τις αλλαγές στην ένταση του ίδιου χρώματος, η μέθοδος τυπικής κλίμακας δίνει καλύτερα αποτελέσματα όταν τα διαλύματα που σχηματίζουν την τυπική κλίμακα διαφέρουν ως προς το χρώμα. Για παράδειγμα, το οργανικό αντιδραστήριο διθιζόνη απουσία μετάλλων μεταπτώσεως έχει καθαρό πράσινο χρώμα, το σύμπλεγμα διθιζόνης με ψευδάργυρο είναι κόκκινο και διαλύματα της τυπικής κλίμακας που περιέχουν διαφορετικές ποσότητες ψευδαργύρου και την ίδια ποσότητα διθειζόνης που λαμβάνεται σε περίσσεια δίνουν όλα τα πιθανά ενδιάμεσα χρώματα μεταξύ πράσινου και κόκκινου. Σε τέτοιες περιπτώσεις, ο προσδιορισμός της συγκέντρωσης των μετάλλων σε μια τυπική κλίμακα δεν είναι κατώτερος σε ακρίβεια από πολλές μεθόδους οργάνων (σφάλμα της τάξης του 10%).
2. Χρωματομετρική ογκομέτρηση.Με μια τέτοια "τιτλοδότηση" δεν συμβαίνουν χημικές αντιδράσεις, το όνομα είναι υπό όρους. Η μέθοδος συνίσταται στο γεγονός ότι ένα έγχρωμο διάλυμα παρασκευάζεται από το δείγμα δοκιμής και χύνεται σε ένα συγκεκριμένο δοχείο και ένα πρότυπο έγχρωμο διάλυμα Χ με γνωστή συγκέντρωση (μεγαλύτερη από ό,τι στο δείγμα) προστίθεται σταδιακά σε άλλο παρόμοιο δοχείο με καθαρό διαλύτη έως ότου τα έγχρωμα διαλύματα δεν είναι ίσα με το μάτι. Δεδομένου ότι το πάχος του απορροφητικού στρώματος είναι το ίδιο, πιστεύεται ότι μετά την εξίσωση των χρωμάτων, η συγκέντρωση του Χ και στα δύο διαλύματα είναι επίσης ίδια. Σύμφωνα με τον όγκο του προτύπου διαλύματος που χρησιμοποιείται, υπολογίζεται πόση από την προς προσδιορισμό ουσία περιείχε το δείγμα.
3. μέθοδος αραίωσης.Στη μέθοδο αυτή παρασκευάζονται επίσης τα δοκιμαστικά και τα τυπικά έγχρωμα διαλύματα και στη συνέχεια αυτό που είναι πιο έντονα χρωματισμένο αραιώνεται με καθαρό διαλύτη μέχρι (με το ίδιο πάχος της στρώσης του διαλύματος!) να εξισωθούν τα ορατά τους χρώματα. Γνωρίζοντας το βαθμό αραίωσης, υπολογίστε τη συγκέντρωση του διαλύματος δοκιμής.
4. Μέθοδος εξισορρόπησης.Η ίδια ένταση απορρόφησης φωτός από τα μελετημένα και τυποποιημένα διαλύματα επιτυγχάνεται εδώ αλλάζοντας το πάχος του στρώματος απορρόφησης. Αυτό μπορεί να γίνει σε μια ειδική συσκευή - ένα χρωματόμετρο εμβάπτισης ή απλά σε ένα ζευγάρι κυλίνδρων, όταν το βλέπουμε από πάνω. Εάν η χημική σύσταση και των δύο διαλυμάτων είναι η ίδια, ο νόμος του Beer ικανοποιείται και τα ορατά χρώματα (και επομένως οι οπτικές πυκνότητες των διαλυμάτων) είναι ίδια, μπορούμε να γράψουμε:
D st \u003d e l st C st D x \u003d e l x C x C x \u003d C st l st / l x
Η μέθοδος εξισορρόπησης είναι πιο ακριβής από άλλες χρωματομετρικές μεθόδους και σας επιτρέπει να βρείτε τη συγκέντρωση του C x με σφάλμα 10-20%.
Αυτή η εργασία περιγράφει μεθόδους για την ανάλυση των φυσικών νερών για την περιεκτικότητα σε διάφορες τοξικές ουσίες και σε όλες τις περιπτώσεις συνιστάται η τυπική μέθοδος κλίμακας. Ωστόσο, με οδηγίες του δασκάλου, η ανάλυση μπορεί να πραγματοποιηθεί με άλλη οπτική μέθοδο. Ας εξετάσουμε τις ιδιότητες ορισμένων τοξικών ουσιών που μπορούν να προσδιοριστούν στα φυσικά νερά με τη χρωματομετρική μέθοδο, καθώς και τις αντιδράσεις σχηματισμού έγχρωμων ενώσεων από αυτές. Αυτές οι αντιδράσεις είναι που θα χρειαστεί να πραγματοποιηθούν κατά τη διάρκεια της εργαστηριακής εργασίας.
Προσδιορισμός φαινολών Οι φαινόλες είναι αρωματικές ενώσεις με μία ή περισσότερες υδροξυλομάδες άμεσα συνδεδεμένες με έναν αρωματικό πυρήνα, όπως έναν δακτύλιο βενζολίου. Εισέρχονται στο περιβάλλον από τα λύματα των βιομηχανικών επιχειρήσεων, ιδιαίτερα των διυλιστηρίων οπτάνθρακα και πετρελαίου. Οι φαινόλες έχουν ισχυρή βιολογική επίδραση. Σε συγκέντρωση φαινολών 0,50 mg/l στο νερό του ποταμού, τα ψάρια πεθαίνουν. Στο πόσιμο νερό στη Ρωσική Ομοσπονδία, η μέγιστη επιτρεπόμενη συγκέντρωση φαινολών ορίζεται σε 0,001 mg/l (από την άποψη της απλούστερης φαινόλης C 6 H 5 OH). Η περιεκτικότητα σε φαινόλες στο πόσιμο νερό, τα φυσικά και τα λύματα ελέγχεται από εργαστήρια της υγειονομικής υπηρεσίας και άλλους οργανισμούς. Για τον προσδιορισμό των φαινολών, χρησιμοποιούνται διάφορες μέθοδοι για τη μετατροπή τους σε έγχρωμες ενώσεις. η επιλογή της μεθόδου ανάλυσης εξαρτάται από τη συγκέντρωση της φαινόλης στο νερό της δοκιμής και την παρουσία παρεμβατικών ουσιών. Μερικές φορές, κατά τη διάρκεια της ανάλυσης, η ποσότητα των φαινολών διαχωρίζεται από τις μη πτητικές παρεμβαλλόμενες ουσίες με απόσταξη των φαινολών από το δείγμα δοκιμής με υδρατμούς· αυτό δεν απαιτείται σε αυτήν την εργασία. Εάν η συγκέντρωση των φαινολών αναμένεται στο επίπεδο των 0,05-50 mg/l (βαριά μολυσμένα νερά), τότε η ανάλυση πραγματοποιείται σύμφωνα με τη μέθοδο Griess χρησιμοποιώντας την αντίδραση με π-νιτροανιλίνη. Αυτό το αντιδραστήριο διαζωτίζεται με νιτρώδες νάτριο εκ των προτέρων (την ημέρα της ανάλυσης) και στη συνέχεια πραγματοποιείται αζωσύζευξη με φαινόλη:
2Η + ® + 2Η 2 Ο
Η προκύπτουσα αζωχρωστική έχει έντονο κίτρινο-καφέ χρώμα. Η συγκέντρωση της χρωστικής θα είναι ανάλογη με τη συγκέντρωση της φαινόλης στο νερό εάν ληφθούν άλλα αντιδραστήρια (νιτρώδη, π-νιτροανιλίνη) σε μεγάλη και ίση περίσσεια. Ο προσδιορισμός είναι μη επιλεκτικός: διαφορετικές φαινόλες δίνουν έγχρωμα προϊόντα παρόμοιες σε ιδιότητες. Η απόδοση των προϊόντων εξαρτάται σε μεγάλο βαθμό από το pH. Η διαζώτωση πραγματοποιείται σε ένα όξινο μέσο και η αζωσύζευξη σε ένα αλκαλικό μέσο.
Όταν κάνετε εργασία, να έχετε κατά νου ότι οι φαινόλες και η π-νιτροανιλίνη είναι τοξικές. Χειριστείτε με προσοχή!
Προσδιορισμός νιτρωδών Η παρουσία αυξημένης συγκέντρωσης νιτρωδών στα φυσικά νερά υποδηλώνει τη ρύπανση τους με οικιακά λύματα. Η περιεκτικότητα σε νιτρώδη άλατα στα φυσικά νερά κυμαίνεται από λίγα μικρογραμμάρια έως δέκατα του mg ανά 1 λίτρο (τα νιτρώδη είναι λιγότερο τοξικά από τις φαινόλες, το MPC είναι 1 mg/l). Για τον προσδιορισμό των νιτρωδών, η πιο συχνά χρησιμοποιούμενη χρωματομετρική μέθοδος βασίζεται στην αντίδραση των νιτρωδών με σουλφανιλικό οξύ και α-ναφθυλαμίνη (αντίδραση Griess-Ilosvay). Πρώτα, τα νιτρώδη που υπάρχουν αντιδρούν με σουλφανιλικό οξύ (αντίδραση διαζωτίωσης), στη συνέχεια το διαζωτισμένο σουλφανιλικό οξύ αντιδρά με α-ναφθυλαμίνη (αντίδραση αζωσύζευξης) και σχηματίζεται μια ερυθρό-ιώδες βαφή:
Δεδομένου ότι και τα δύο αντιδραστήρια εισάγονται σε μεγάλη περίσσεια σε σύγκριση με τα νιτρώδη, η συγκέντρωση της χρωστικής και η οπτική πυκνότητα του διαλύματός της εξαρτώνται μόνο από τη συγκέντρωση των νιτρωδών. Ο νόμος της μπύρας γενικά ισχύει. Το όριο ανίχνευσης νιτρωδών χωρίς πρόσθετη συγκέντρωση είναι 1 mg/l. Παρεμβαίνουν ισχυροί οξειδωτικοί και αναγωγικοί παράγοντες.
Προσδιορισμός χλωρίου Η περιεκτικότητα σε «ενεργό χλώριο» προσδιορίζεται κατά την ανάλυση του χλωριωμένου νερού της βρύσης. Το διαλυμένο χλώριο προσδιορίζεται επίσης σε ορισμένα λύματα, MPC C l \u003d 0,4 mg / l. Εκτός από τα μόρια Cl 2, η έννοια του "ενεργού χλωρίου" περιλαμβάνει επίσης μια σειρά από άλλες ασταθείς ενώσεις χλωρίου που σχηματίζονται κατά τη χλωρίωση του νερού, για παράδειγμα, υποχλωριώτες, χλωραμίνες κ.λπ. Όλες αυτές οι ενώσεις αντιδρούν σαν ελεύθερο χλώριο και προσδιορίζονται συνολικά . Το αποτέλεσμα της ανάλυσης εκφράζεται σε όρους Cl 2 (mg/l). Ο προσδιορισμός πρέπει να πραγματοποιείται αμέσως μετά τη δειγματοληψία του νερού.
Για τον προσδιορισμό μικρών ποσοτήτων χλωρίου, η χρωματομετρική μέθοδος με ο-τολουιδίνη είναι πιο βολική. Αυτό το αντιδραστήριο οξειδώνεται από το χλώριο (καθώς και άλλους οξειδωτικούς παράγοντες) με έναν μηχανισμό που δεν είναι πλήρως κατανοητός και το διάλυμα γίνεται κίτρινο ή πορτοκαλί. Ο σίδηρος (>0,3 mg/l) και τα νιτρώδη (>0,1 mg/l) παρεμβαίνουν στον προσδιορισμό. Με την παρουσία ενός αριθμού παρεμβατικών ουσιών, ο προσδιορισμός του χλωρίου είναι πολύ περίπλοκος. Οι κατάλληλες τεχνικές περιγράφονται στη βιβλιογραφία.
Δεδομένου ότι η τυπική ζυγαριά που περιέχει οξειδωμένη ο-τολουιδίνη είναι ασταθής κατά την αποθήκευση και δεν είναι επιθυμητό να παρασκευάζεται ξανά καθημερινά, τα εργαστήρια χρησιμοποιούν συχνά μια σταθερή τεχνητή ζυγαριά που παρασκευάζεται από διαλύματα K 2 CrO 4 και K 2 Cr 2 O 7 . Το χρώμα των τυποποιημένων διαλυμάτων αυτής της κλίμακας αντιστοιχεί ακριβώς στο χρώμα των διαλυμάτων που περιέχουν διάφορες γνωστές ποσότητες του προϊόντος αντίδρασης χλωρίου με ο-τολουιδίνη. Τέτοιες τεχνητές κλίμακες χρησιμοποιούνται αρκετά συχνά στην πράξη.
Η χρωματομετρία ως μέθοδος χημικής ανάλυσης χρησιμοποιείται για τον προσδιορισμό της συγκέντρωσης μιας συγκεκριμένης ουσίας σε ένα διάλυμα. Η μέθοδος σάς επιτρέπει να εργαστείτε με έγχρωμα διαλύματα ή διαλύματα που μπορούν να γίνουν έγχρωμα ως αποτέλεσμα μιας συγκεκριμένης χημικής αντίδρασης.
Βασικές αρχές χρωματομετρίας
Οι μέθοδοι χημικής ανάλυσης που χρησιμοποιούν χρωματομετρία βασίζονται στο νόμο Bouguer-Lambert-Veer, ο οποίος δηλώνει ότι η ένταση του χρώματος εξαρτάται από τη συγκέντρωση της έγχρωμης ουσίας στο διάλυμα και από το πάχος του υγρού στρώματος.
Χρησιμοποιώντας διάφορες χρωματομετρικές τεχνικές, είναι δυνατό να εκτιμηθεί η ποσοτική περιεκτικότητα ορισμένων ουσιών σε ένα διάλυμα με αρκετά υψηλή ακρίβεια - συνήθως είναι 0,1-1%. Αυτή η ακρίβεια, κατά κανόνα, δεν είναι κατώτερη από την ακρίβεια με την οποία καθορίζονται οι συγκεντρώσεις ως αποτέλεσμα πολύ πιο περίπλοκων και δαπανηρών χημικών αναλύσεων και επαρκεί για πολλές εργασίες - όχι μόνο βιομηχανικές, αλλά και ειδικού χαρακτήρα. Οι χρωματομετρικές μέθοδοι μπορούν να προσδιορίσουν τη συγκέντρωση ουσιών έως και 10−8 mol/l.
Οι χρωματομετρικές μέθοδοι χρησιμοποιούν οπτική σύγκριση ή σύγκριση χρησιμοποιώντας όργανα - φωτοχρωμόμετρα ή φασματοφωτόμετρα. Η σύγκριση γίνεται με άμεσες ή αντισταθμιστικές μεθόδους.
άμεση μέθοδος
 Η άμεση μέθοδος περιλαμβάνει τη σύγκριση του βαθμού χρωματισμού του διαλύματος δοκιμής σε μια ορισμένη θερμοκρασία και σε ένα συγκεκριμένο υγρό στρώμα με ένα διάλυμα αναφοράς. Το πρότυπο περιέχει μια επακριβώς γνωστή ποσότητα χρωστικής ουσίας στην ίδια θερμοκρασία και στο ίδιο υγρό στρώμα.
Η άμεση μέθοδος περιλαμβάνει τη σύγκριση του βαθμού χρωματισμού του διαλύματος δοκιμής σε μια ορισμένη θερμοκρασία και σε ένα συγκεκριμένο υγρό στρώμα με ένα διάλυμα αναφοράς. Το πρότυπο περιέχει μια επακριβώς γνωστή ποσότητα χρωστικής ουσίας στην ίδια θερμοκρασία και στο ίδιο υγρό στρώμα.
Μερικές φορές γίνεται σύγκριση με απεσταγμένο νερό. Κατά κανόνα, τέτοιες μέθοδοι βασίζονται στη χρήση φωτοχρωμομέτρων ή φασματοφωτομέτρων. Αυτές οι συσκευές μετρούν την ισχύ του ρεύματος, ανάλογα με την ένταση του εκπεμπόμενου φωτός που διέρχεται από το διάλυμα δοκιμής.
Η ακρίβεια της μέτρησης υλικού είναι μεγαλύτερη από την οπτική. Χρησιμοποιείται επίσης μια οπτική μέθοδος για τη σύγκριση της χρωματικής έντασης του διαλύματος με διαλύματα αναφοράς, η συγκέντρωση της ουσίας στην οποία είναι γνωστή.
Μέθοδος αποζημίωσης
Η μέθοδος αντιστάθμισης βασίζεται στη μεταφορά του χρώματος του δείγματος δοκιμής στο αντίστοιχο χρώμα. Λύσεις, χρησιμοποιώντας διάφορες οπτικές συσκευές - καθρέφτες, γυαλιά και πρίσματα, τοποθετούνται στη συσκευή με τέτοιο τρόπο ώστε να συνδυάζονται στο οπτικό πεδίο του ερευνητή. Το μάτι είναι ικανό να καθορίσει τον ίδιο χρωματισμό δύο δειγμάτων με υψηλή ακρίβεια. Σε ορισμένες συσκευές, η εργασία διευκολύνεται από το γεγονός ότι όταν η ένταση του χρώματος συμπίπτει, το οπτικό όριο που αρχικά χωρίζει τις λύσεις εξαφανίζεται.
Προκειμένου να φέρει το διάλυμα που μελετήθηκε στο διάλυμα αναφοράς, προστίθεται σε αυτό ένας διαφανής διαλύτης ή αυξάνεται το ύψος του υγρού στρώματος. Στη συνέχεια, από την τιμή του προστιθέμενου αραιωτικού ή το ύψος της στιβάδας του διαλύματος, προκύπτει ένα ποσοτικό χαρακτηριστικό της συγκέντρωσης των χρωστικών στο διάλυμα. Οι μέθοδοι αντιστάθμισης χρησιμοποιούνται σε οπτικά χρωματόμετρα και φωτοχρωμόμετρα. Είναι τα πιο πρακτικά, αφού δεν επηρεάζονται από εξωτερικούς παράγοντες - για παράδειγμα, τη θερμοκρασία.
Πότε και πού εφαρμόζονται οι χρωματομετρικές μέθοδοι;
Οι χρωματομετρικές μέθοδοι για χημική ανάλυση χρησιμοποιούνται σε περιπτώσεις όπου είναι γνωστή η ακριβής χημική σύνθεση του διαλύματος. το διάλυμα είναι διαφανές. υπάρχει δείγμα αναφοράς. οι θερμοκρασίες του δείγματος και του διαλύματος δοκιμής είναι ίσες. Με τη βοήθεια αυτών των μεθόδων, είναι δυνατός ο προσδιορισμός της συγκέντρωσης των ουσιών σε άχρωμα διαλύματα, εάν είναι δυνατό να γίνει το διάλυμα έγχρωμο με την προσθήκη ενός συγκεκριμένου αντιδραστηρίου.
Η χρωματομετρία χρησιμοποιείται:
Στην αναλυτική χημεία?
- στην ιατρική (περιεκτικότητα σε αίμα).
- για τον έλεγχο της ποιότητας του πόσιμου νερού και των λυμάτων.
- στη βιομηχανία τροφίμων για τον προσδιορισμό του βαθμού καθαρισμού του κρασιού, της μπύρας, της ζάχαρης.
- στη βιομηχανία - να αναλύσει τη σύνθεση λιπαντικών ελαίων, κηροζίνης.
Πλεονεκτήματα των χρωματομετρικών μεθόδων:
Απλότητα;
- δεν χρειάζεται ακριβός εξοπλισμός.
- αποτελεσματικότητα των μετρήσεων, δυνατότητα διεξαγωγής αναλύσεων απευθείας στην παραγωγή.
- τη δυνατότητα προσδιορισμού πολύ μικρών συγκεντρώσεων ουσιών που είναι δύσκολο να υπολογιστούν με άλλες μεθόδους χημικής ανάλυσης.
Στο κατάστημα εργαστηριακών υαλικών και χημικού εξοπλισμού «PrimeChemicalsGroup» μπορείτε επίσης να αγοράσετε χρωματομετρικούς δοκιμαστικούς σωλήνες διαφόρων μεγεθών σε προσιτές τιμές. Πραγματοποιούμε παράδοση σε όλη τη Μόσχα και την περιοχή της Μόσχας.
- Σε επαφή με 0
- Google Plus 0
- Εντάξει 0
- Facebook 0